��Ŀ����
������ʵ��д�����з�Ӧ���Ȼ�ѧ��Ӧ����ʽ��
��1����25�桢101kPa�£�1g�״���ȫȼ������CO2��Һ̬ˮʱ����22��68kJ�����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ ��
��2����������N2��O2��ȫ��Ӧ��ÿ����23gNO2��Ҫ����16��95kJ���������ʾ�÷�Ӧ���Ȼ�ѧ����ʽΪ ��
��3����NA��ʾ�����ӵ���������C2H2����̬����ȫȼ������CO2��Һ̬ˮ�ķ�Ӧ�У�ÿ��5NA������ת��ʱ���ų�650kJ�����������ʾ�÷�Ӧ���Ȼ�ѧ����ʽΪ _________________________________________________��
��4����֪��1molH��H����1molN��H����1molN��N���ֱ���Ҫ��������436kJ��391kJ��946kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ ��
��1����25�桢101kPa�£�1g�״���ȫȼ������CO2��Һ̬ˮʱ����22��68kJ�����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ ��
��2����������N2��O2��ȫ��Ӧ��ÿ����23gNO2��Ҫ����16��95kJ���������ʾ�÷�Ӧ���Ȼ�ѧ����ʽΪ ��
��3����NA��ʾ�����ӵ���������C2H2����̬����ȫȼ������CO2��Һ̬ˮ�ķ�Ӧ�У�ÿ��5NA������ת��ʱ���ų�650kJ�����������ʾ�÷�Ӧ���Ȼ�ѧ����ʽΪ _________________________________________________��
��4����֪��1molH��H����1molN��H����1molN��N���ֱ���Ҫ��������436kJ��391kJ��946kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ ��
��1��CH3OH��l��+1��5O2��g���TCO2��g��+2H2O��l����H=-725��8 kJ?mol-1��
��2��N2��g��+2O2��g��=2NO2��g����H=+67��8kJ?mol-1��
��3��C2H2��g��+O2��g����2CO2��g��+H2O��l����H=-1300kJ?mol-1��
��4��N2��g��+3H2��g�� 2NH3��g����H=-92kJ?mol-1��
2NH3��g����H=-92kJ?mol-1��
��2��N2��g��+2O2��g��=2NO2��g����H=+67��8kJ?mol-1��
��3��C2H2��g��+O2��g����2CO2��g��+H2O��l����H=-1300kJ?mol-1��
��4��N2��g��+3H2��g��
 2NH3��g����H=-92kJ?mol-1��
2NH3��g����H=-92kJ?mol-1�������������1����25�桢101kPa�£�1g�״���CH3OH��ȼ������CO2��Һ̬ˮʱ����22��68kJ��1mol�״���ȫȼ�����ɶ�����̼��Һ̬ˮ����Ϊ22��68kJ��32=725��8KJ�����Լ״�ȼ���ȵ��Ȼ�ѧ����ʽΪCH3OH��l��+1��5O2��g���TCO2��g��+2H2O��l����H=-725��8 kJ?mol-1��
��2��������N2��O2��ȫ��Ӧ��ÿ����23��NO2��Ҫ����16��95kJ����������ÿ����92��NO2��Ҫ����67��8kJ���������Ȼ�ѧ����ʽΪN2��g��+2O2��g��=2NO2��g����H=+67��8kJ?mol-1��
��3����3����C2H2����̬����ȫȼ������CO2��Һ̬ˮ�ķ�Ӧ�У�ÿ��5NA������ת��ʱ���ų�650kJ��������������10NA������ת��ʱ���ų�1300kJ��������
���Ȼ�ѧ����ʽΪ��C2H2��g��+2��5O2��g����2CO2��g��+H2O��l����H=-1300kJ?mol-1��
��4���ڷ�ӦN2+3H2?2NH3�У�����3molH-H����1molN��N�������յ�����Ϊ3��436kJ+946kJ=2254kJ������2molNH3�����γ�6molN-H�����ų�������Ϊ6��391kJ=2346kJ�����յ������٣��ų��������࣬�÷�ӦΪ���ȷ�Ӧ���ų�������Ϊ2346kJ-2254kJ=92kJ��N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��
 2NH3��g����H=-92kJ?mol-1��
2NH3��g����H=-92kJ?mol-1��
��ϰ��ϵ�д�
�����Ŀ








 2NO(g��
2NO(g��  H��0
H��0 2 Na2CO3��l��+ C(s,���ʯ) ��H=��1080��9kJ/mol
2 Na2CO3��l��+ C(s,���ʯ) ��H=��1080��9kJ/mol

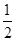 H2(g)+
H2(g)+  2NO2(g) ��H ����ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g) ��H ����ϵ�У�n(NO)��ʱ��ı仯����� CH3OH(g)��ͼ1��ʾ��Ӧ�е������仯��ͼ2��ʾһ���¶��£������Ϊ1L���ܱ������м���2mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��
CH3OH(g)��ͼ1��ʾ��Ӧ�е������仯��ͼ2��ʾһ���¶��£������Ϊ1L���ܱ������м���2mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��
 CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ ���ﵽƽ��������������������䣬���������ѹ��Ϊ0.5L����ƽ�� �ƶ� (�������������)��
CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ ���ﵽƽ��������������������䣬���������ѹ��Ϊ0.5L����ƽ�� �ƶ� (�������������)��
 FeO(s) +CO(g) ��H ="a" kJ/mol
FeO(s) +CO(g) ��H ="a" kJ/mol 
 H= ?241��8kJ/mol
H= ?241��8kJ/mol  2SO3(g)��
2SO3(g)�� 2NO(g)
2NO(g)