题目内容
已知反应:CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
在427°C时的平衡常数是9.4.如果反应开始时,一氧化碳和水蒸气的浓度都是0.01mol·L-1,计算一氧化碳在此反应条件下的转化率。
 H2(g)+CO2(g)
H2(g)+CO2(g)在427°C时的平衡常数是9.4.如果反应开始时,一氧化碳和水蒸气的浓度都是0.01mol·L-1,计算一氧化碳在此反应条件下的转化率。
75.4﹪
试题分析:CO(g)+H2O(g)
 H2(g)+CO2(g)
H2(g)+CO2(g)起始:0.01mol/L 0.01mol/L 0 0
转化: x x x x
平衡0.01-x 0.01-x x x
依题意有:
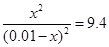 解之得:x=0.754mol
解之得:x=0.754mol因此一氧化碳在此反应条件下的转化率为:
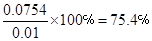

练习册系列答案
相关题目
 2HI(g) ΔH =" -14.9" kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)="0.008" mol/L。 下列判断正确的
2HI(g) ΔH =" -14.9" kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)="0.008" mol/L。 下列判断正确的 2NH3已达到平衡,下列有关说法正确的 ( )
2NH3已达到平衡,下列有关说法正确的 ( ) 2CrO42-(黄色)+2H+,
2CrO42-(黄色)+2H+, Z(g)+2W(g) ΔH<0,达到平衡(Ⅰ)时,V(B)=0.8a L。
Z(g)+2W(g) ΔH<0,达到平衡(Ⅰ)时,V(B)=0.8a L。
 pC(g)+qD(g);△H<0.下列结论中不正确的是
pC(g)+qD(g);△H<0.下列结论中不正确的是 HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 2 HBr(g) ΔH<0平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是( )
2 HBr(g) ΔH<0平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是( ) zC(g)。达到平衡后,测得A气体的浓度为0.5mol/L。当恒温下将密闭容器的容积扩大到原来的二倍,再达平衡后,测得A的浓度为0.3mol/L。下列叙述正确的是
zC(g)。达到平衡后,测得A气体的浓度为0.5mol/L。当恒温下将密闭容器的容积扩大到原来的二倍,再达平衡后,测得A的浓度为0.3mol/L。下列叙述正确的是