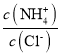题目内容
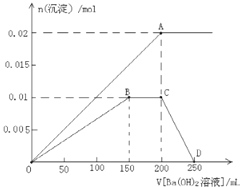
【题目】将2molNaHCO3和一定量的Na2O2固体混合,在加热的条件下使其反应,经测定无Na2O2剩余,则最后所得固体的物质的量(n)为
A.1mol<n≤2molB.1mol<n≤4molC.2mol<n≤4molD.n>4mol
【答案】B
【解析】
发生的反应方程式是:2NaHCO3![]() Na2CO3+CO2↑+H2O;2Na2O2+2H2O=4NaOH+ O2↑;2Na2O2+2CO2 =2Na2CO3+ O2。2molNaHCO3分解产生1mol的Na2CO3,1mol的CO2和1mol的H2O。CO2和H2O同时存在时,可以认为CO2先和Na2O2反应。若Na2O2不足量,产生的CO2没有完全消耗,此时固体的物质的量大于1mol;若Na2O2恰好完全与产生的CO2发生反应,则又产生固体Na2CO3的物质的量是1mol,此时所得固体的物质的量为2mol;若CO2反应完后还有Na2O2剩余,则Na2O2接着与水发生反应,若Na2O2和产生的1mol水完全反应,则产生的固体NaOH物质的量是2mol,此时反应后固体的总物质的量是4mol;所以反应后固体的物质的量介于1mol和4mol之间,因此选项是B。
Na2CO3+CO2↑+H2O;2Na2O2+2H2O=4NaOH+ O2↑;2Na2O2+2CO2 =2Na2CO3+ O2。2molNaHCO3分解产生1mol的Na2CO3,1mol的CO2和1mol的H2O。CO2和H2O同时存在时,可以认为CO2先和Na2O2反应。若Na2O2不足量,产生的CO2没有完全消耗,此时固体的物质的量大于1mol;若Na2O2恰好完全与产生的CO2发生反应,则又产生固体Na2CO3的物质的量是1mol,此时所得固体的物质的量为2mol;若CO2反应完后还有Na2O2剩余,则Na2O2接着与水发生反应,若Na2O2和产生的1mol水完全反应,则产生的固体NaOH物质的量是2mol,此时反应后固体的总物质的量是4mol;所以反应后固体的物质的量介于1mol和4mol之间,因此选项是B。

【题目】在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g) ![]() Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法正确的是( )
A. 上述生成Ni(CO)4(g)的反应为吸热反应
B. 25 ℃时反应Ni(CO)4(g) ![]() Ni(s)+4CO(g)的平衡常数为0.5
Ni(s)+4CO(g)的平衡常数为0.5
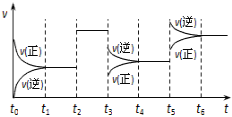
C. 在80 ℃时,测得某时刻,Ni(CO)4、CO浓度均0.5 mol/L,则此时v正>v逆
D. 80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol/L
【题目】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。请填写下列空白:
(1)滴定终点的判断:溶液由_____________。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是(_____)
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
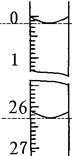
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为_________mL。
(4)某学生根据3次实验分别记录有关数据如表:
滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000 mol/L盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 平均耗用盐酸 体积/mL | ||
第一次 | 25.00 | 0.00 | 26.15 | ①V=__________ |
第二次 | 25.00 | 0.56 | 30.30 | |
第三次 | 25.00 | 0.20 | 26.35 | |
②依据上表数据计算该NaOH溶液的物质的量浓度________ (计算结果取4位有效数)。