题目内容
液氨和水类似,也能电离:2NH3?NH4++NH2-,某温度时,其离子积K=2×l0-30.该温度下:
①将少量NH4Cl固体加入液氨中,K 2×10-30(填“<”、“>”或“=”);
②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒的浓度大小关系为: .
①将少量NH4Cl固体加入液氨中,K
②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒的浓度大小关系为:
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:①K是温度的函数,温度不变K值不变;
②将少量金属钠投入液氨中,2NH4++2Na=NH3↑+2Na++H2↑,导致平衡正向移动,所以离子浓度大小关系为:c(NH3)>c(NH2-)>c(Na+)>c(NH4+).
②将少量金属钠投入液氨中,2NH4++2Na=NH3↑+2Na++H2↑,导致平衡正向移动,所以离子浓度大小关系为:c(NH3)>c(NH2-)>c(Na+)>c(NH4+).
解答:
解:①K是温度的函数,温度不变K值不变,故答案为:=;
②将少量金属钠投入液氨中,2NH4++2Na=NH3↑+2Na++H2↑,导致平衡正向移动,所以离子浓度大小关系为:c(NH3)>c(NH2-)>c(Na+)>c(NH4+),
故答案为:c(NH3)>c(NH2-)>c(Na+)>c(NH4+).
②将少量金属钠投入液氨中,2NH4++2Na=NH3↑+2Na++H2↑,导致平衡正向移动,所以离子浓度大小关系为:c(NH3)>c(NH2-)>c(Na+)>c(NH4+),
故答案为:c(NH3)>c(NH2-)>c(Na+)>c(NH4+).
点评:本题考查弱电解质的电离平衡,学生学会类推法的应用,比较简单.

练习册系列答案
相关题目
已知,25℃时有关弱酸的电离平衡常数如下表:下列有关说法正确的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7,K2=5.6×l0-11 |
| A、测得1000mL 0.50mol/L盐酸与1000mL 0.55mol/L NaOH溶液混合时放出28.65kJ的热量,则稀醋酸和稀NaOH溶液反应的△H=-57.3kJ?mol-1 | ||
| B、冰醋酸中逐滴加水,溶液的导电性和pH、醋酸的电离程度均先增大后减小 | ||
| C、向NaCN溶液中通入少量CO2:2CN-+CO2+H2O═2HCN+CO32- | ||
D、将0.1mol/L的醋酸溶液加水稀释,则
|
某小组设计如图装置(盐桥中盛有浸泡了KNO3溶液的琼脂)研究电化学原理.下列叙述正确的是( )
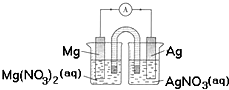

| A、银片为负极,发生的反应为:Ag++e-=Ag |
| B、进行实验时,琼脂中K+移向Mg(NO3)2溶液 |
| C、用稀硫酸代替AgNO3溶液,可形成原电池 |
| D、取出盐桥,电流表依然有偏转 |
 四种有机物
四种有机物 能源的开发利用与人类社会的可持续发展息息相关.
能源的开发利用与人类社会的可持续发展息息相关.