题目内容
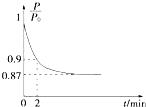 能源的开发利用与人类社会的可持续发展息息相关.
能源的开发利用与人类社会的可持续发展息息相关.已知:Fe2O3(s)+3C(s)═2Fe(s)+3CO(g)△H1=a kJ?mol-1
CO(g)+
| 1 |
| 2 |
4Fe(s)+3O2(g)═2Fe2O3(s)△H3=c kJ?mol-1
则C的燃烧热△H=
考点:反应热和焓变
专题:化学反应中的能量变化
分析:三个热化学方程式依次编号为①、②、③,根据盖斯定律,(①×2+②×6+③)÷6得,C(s)+O2(g)═CO2(g)△H=
(2a+6b+c)kJ?mol-1,则C的燃烧热为
kJ?mol-1.
| 1 |
| 6 |
| 2a+6b+c |
| 6 |
解答:
解:已知:①Fe2O3(s)+3C(s)═2Fe(s)+3CO(g)△H1=a kJ?mol-1
②CO(g)+
O2(g)═CO2(g)△H2=b kJ?mol-1
③4Fe(s)+3O2(g)═2Fe2O3(s)△H3=c kJ?mol-1
据盖斯定律,(①×2+②×6+③)÷6得:C(s)+O2(g)═CO2(g)△H=
(2a+6b+c)kJ?mol-1,则C的燃烧热为
kJ?mol-1,故答案为:
.
②CO(g)+
| 1 |
| 2 |
③4Fe(s)+3O2(g)═2Fe2O3(s)△H3=c kJ?mol-1
据盖斯定律,(①×2+②×6+③)÷6得:C(s)+O2(g)═CO2(g)△H=
| 1 |
| 6 |
| 2a+6b+c |
| 6 |
| 2a+6b+c |
| 6 |
点评:本题考查盖斯定律和燃烧热的概念,题目难度不大.

练习册系列答案
相关题目
将如图所示实验装置的K闭合,下列判断错误的是( )
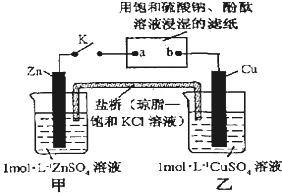

| A、盐桥中的K+移向乙池 |
| B、电子沿Zn→a→b→Cu路径流动 |
| C、b电极上的反应式为4OH-4e-=O2↑+2H2O |
| D、片刻后可观察到滤纸a点变红色 |
下列说法中,不正确的是( )
| A、NH3的水溶液可以导电,说明NH3是电解质 |
| B、明矾水解形成Al(OH)3胶体有吸附性,可用于水的净化 |
| C、二氧化硅可用于制造光导纤维 |
| D、向淀粉碘化钾溶液中加溴水,溶液变为蓝色,说明Br2的氧化性强于I2 |
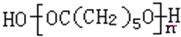
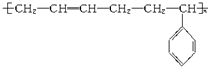
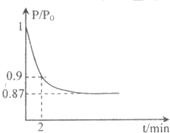 某实验小组模拟工业合成氨,利用合成的氨气验证氨气具有还原性实验.
某实验小组模拟工业合成氨,利用合成的氨气验证氨气具有还原性实验.