题目内容
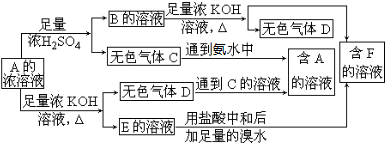
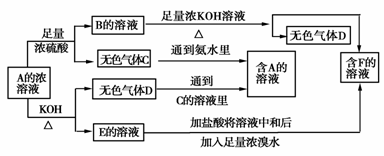
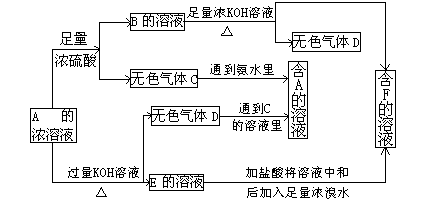
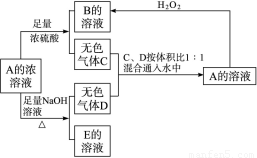
从某物质A的水溶液出发,有下图所示的一系列变化(参加反应或反应生成的H2O没有表示出来)。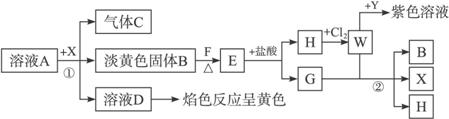
试完成下列问题:
(1)写出下列物质的化学式(或名称):
A___________,E___________,X___________,Y___________。
(2)写出步骤①、②反应的离子方程式:
①_________________________________________________
②_________________________________________________
(1)Na2S2O3 FeS HCl C6H5OH
(2)![]() +2H+=S↓+SO2↑+H2O
+2H+=S↓+SO2↑+H2O
2Fe3++H2S=2Fe2++S↓+2H+
解析:此题的突破口是破译“紫色溶液”,该溶液显然不是KMnO4溶液。分析“H+Cl2→W![]() 紫色溶液”,可知“H+Cl2→W”为化合反应,并且考虑到三价铁遇苯酚显紫色。这使我们联想到常见的反应2FeCl2+Cl2====2FeCl3,由上易知,H为氯化亚铁,W为氯化铁,Y为苯酚。由G+W(FeCl3)→B(淡黄色固体)+X+H(FeCl2)又知,其中G为还原剂,固体B为反应后的生成物,这使我们联想到H2S与FeCl3的反应,从而可断定G为H2S,B为S,X为HCl。“B(S)+F
紫色溶液”,可知“H+Cl2→W”为化合反应,并且考虑到三价铁遇苯酚显紫色。这使我们联想到常见的反应2FeCl2+Cl2====2FeCl3,由上易知,H为氯化亚铁,W为氯化铁,Y为苯酚。由G+W(FeCl3)→B(淡黄色固体)+X+H(FeCl2)又知,其中G为还原剂,固体B为反应后的生成物,这使我们联想到H2S与FeCl3的反应,从而可断定G为H2S,B为S,X为HCl。“B(S)+F![]() E
E![]() H(FeCl2)+G(H2S)”中的F为铁,E为硫化亚铁。“A+X(HCl)→B(S)+C(气体)+D”中的A为硫代硫酸钠,C为SO2,D为NaCl。反应①的离子方程式为:
H(FeCl2)+G(H2S)”中的F为铁,E为硫化亚铁。“A+X(HCl)→B(S)+C(气体)+D”中的A为硫代硫酸钠,C为SO2,D为NaCl。反应①的离子方程式为:![]() +2H+====S↓+SO2↑+H2O,反应②的离子方程式为:2Fe3++H2S====2Fe2++S↓+2H+。
+2H+====S↓+SO2↑+H2O,反应②的离子方程式为:2Fe3++H2S====2Fe2++S↓+2H+。

练习册系列答案
相关题目