题目内容
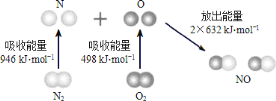
【题目】氢气是未来最理想的能源之一,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O![]() 2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:
2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:
(1)海水分解生成的氢气用于燃料电池时,实现____能转变为____能。水分解时,断裂的化学键为____键,(填极性共价,非极性共价或离子)分解海水的反应属于_____反应(填“放热”或“吸热”)。
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:A极:2H2+2O2--4e-===2H2O;B极:O2+4e-===2O2-,则A极是电池的____极;电子从该极_____(填“流入”或“流出”)。电流从该电极_____(填“流入”或“流出”)
(3)有人以化学反应:2Zn+O2+4H+===2Zn2++2H2O为基础设计出一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是____,正极上发生反应的电极反应式为____。
【答案】化学 电 极性共价 吸热 负 流出 流入 Zn O2+4H++4e-=2H2O
【解析】
(1)原电池是将化学能转化为电能的装置,非金属元素之间形成的化学键大多是共价键,物质的分解反应是吸热反应;
(2)中性或弱酸性条件下,钢铁发生吸氧腐蚀,负极上铁失电子发生氧化反应;铁与水和氧气同时接触时容易生锈,因此隔绝水和氧气可以防止铁制品生锈。
(1)海水分解生成的氢气用于燃料电池,燃料电池是将化学能转化为电能的装置,水分解时,断裂的化学键为HO键,属于极性共价键,分解海水的反应属于吸热反应,
故答案为:化学;电;极性共价;吸热;
(2) 由A极的电极反应式2H2+2O2--4e-===2H2O可知,A电极上发生的是氧化反应,所以A极是电池的负极,电子从负极流出,而电流与电子的流向相反,所以流入A极,
故答案为:负;流出;流入;
(3)由总反应2Zn+O2+4H+===2Zn2++2H2O看,电解质溶液为酸性环境,反应中锌被氧化为锌离子,所以原电池的负极材料是锌,正极氧气得电子转化为水,发生反应的电极反应式为O2+4H++4e-=2H2O,
故答案为:Zn;O2+4H++4e-=2H2O。

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案