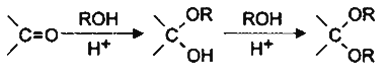
题目内容
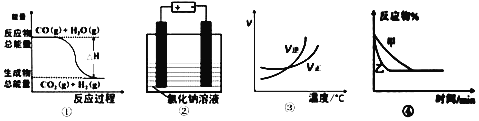
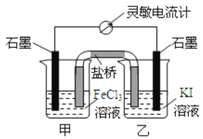
【题目】如图,电源A是氢氧燃料电池(电解质溶液为KOH溶液),B为浸透饱和氯化钠溶液的pH试纸,甲为电解池。请填空:
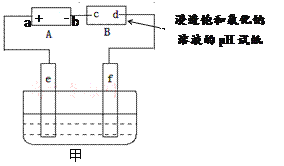
(1)电源A中a极应通入的气体是______,b极上发生的电极反应是_______________。
(2)通电后,试纸上c极称为_____极,实验中发现该极周围pH试纸变蓝色,原因是_____(结合电极反应式说明)。
(3)实验中d极周围可能观察到的现象是的______________________________。
(4)①若利用甲实现铁上镀锌,应将铁接_________极(填“e”或“f”);
②若利用甲实现粗铜的精炼,f电极上的反应是_____________________________。
【答案】 O2 H2-2e-+2OH-=2H2O 阴 发生反应2H2O+2e-=H2+2OH-,该电极周围溶液呈碱性 电极周围先变红,后由电极中心向外慢慢褪色 f Cu2++2e-=Cu
【解析】本题主要考查原电池和电解池原理。
(1)电源A中a极作正极,发生还原反应,应通入的气体是氧气,b极上发生的电极反应是H2-2e-+2OH-=2H2O。
(2)通电后,试纸上c极与负极相连,称为阴极,实验中发现该极周围pH试纸变蓝色,原因是:发生反应2H2O+2e-=H2+2OH-,该电极周围溶液呈碱性。
(3)实验中d极产生氯气,氯气遇水产生盐酸和次氯酸,pH试纸先在盐酸作用下变红,后在次氯酸作用下被漂白而褪色,所以d极周围可能观察到的现象是:电极周围先变红,后在次氯酸由电极中心向外慢慢褪色。
(4)①若利用甲实现铁上镀锌,应将铁接阴极f极;
②若利用甲实现粗铜的精炼,f电极上发生还原反应,反应是Cu2++2e-=Cu。

 小题狂做系列答案
小题狂做系列答案【题目】化学实验是进行化学研究的有效方法,请回答下列实验中的有关问题。
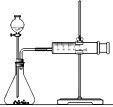
I.用如图所示的装置测定中和热。

实验药品:100mL 0.50 molL-1盐酸、100mL 0.55 molL-1NaOH溶液。
实验步骤:略。
回答下列问题:
(1)从实验装置上看,还缺少环形玻璃搅拌棒,该装置的作用是____________;有同学提议可以用铜质搅拌棒替代,你是否赞同(说明理由)________________。
(2)你认为该实验成功的关键是______________________________。
II.影响化学反应速率的因素很多,某校课外兴趣小组用实验的方法进行探究。甲、乙两个兴趣小组利用Mg、Fe、Cu和不同浓度的硫酸(0.5 molL-1、2 molL-1、18.4 molL-1),设计实验方案来研究影响反应速率的因素。
(1)请帮助甲小组完成研究的实验报告:
实 验 步 骤 | 现 象 | 结 论 |
①分别取等体积0.5 molL-1硫酸于试管中 ②分别投入大小、形状相同的Mg、Fe、Cu ③观察金属表面产生气体的快慢 | ①产生气体的速率Mg>Fe ②Cu上无气体产生 | _________ |
根据控制变量法,要得出正确的实验结论,在实验过程中需要保持温度和压强相同。
(2)乙小组为了更精确地研究浓度对反应速率的影响,利用右图装置进行定量实验。该小组选用的实验药品是:Fe、2molL-1硫酸和______molL-1硫酸。