题目内容
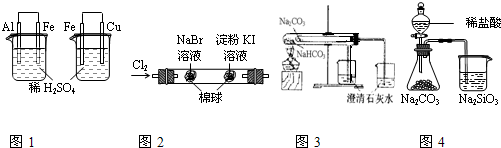
Cl2、Br2、I2都具有氧化性,其氧化性Cl2>Br2>I2,Cl2能把溴从溴化物中置换出来,其余依此类推.请据此写出下列置换反应的化学方程式.
(1)将氯气分别通入KBr溶液和KI溶液中
(2)将溴水滴入KI溶液中
(1)将氯气分别通入KBr溶液和KI溶液中
Cl2+2KBr═2KCl+Br2
Cl2+2KBr═2KCl+Br2
、Cl2+2KI═2KCl+I2
Cl2+2KI═2KCl+I2
.(2)将溴水滴入KI溶液中
Br2+2KI═2KBr+I2
Br2+2KI═2KBr+I2
.分析:根据题干中所提供的信息来考虑即可:氧化性强的非金属单质可以把氧化性弱的非金属单质从盐溶液中置换出来.
解答:解:(1)已知氧化性Cl2>Br2>I2氧化性强的非金属单质可以把氧化性弱的非金属单质从盐溶液中置换出来,所以将氯气分别通入KBr溶液和KI溶液中
分别反应生成Br2和I2,其反应的化学方程式为:Cl2+2KBr═2KCl+Br2;Cl2+2KI═2KCl+I2;
故答案为:Cl2+2KBr═2KCl+Br2;Cl2+2KI═2KCl+I2;
(2)Br2与KI反应生成物是溴化钾和碘,用观察法配平即可,其反应方程式为:Br2+2KI═2KBr+I2,故答案为:Br2+2KI═2KBr+I2.
分别反应生成Br2和I2,其反应的化学方程式为:Cl2+2KBr═2KCl+Br2;Cl2+2KI═2KCl+I2;
故答案为:Cl2+2KBr═2KCl+Br2;Cl2+2KI═2KCl+I2;
(2)Br2与KI反应生成物是溴化钾和碘,用观察法配平即可,其反应方程式为:Br2+2KI═2KBr+I2,故答案为:Br2+2KI═2KBr+I2.
点评:本题考查了卤素单质间的置换反应,题目比较简单,注意根据氧化性强的非金属单质可以把氧化性弱的非金属单质从盐溶液中置换出来分析.

练习册系列答案
 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
(2012?上海)图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O 对实验现象的“解释或结论”正确的是( )
|
卤素单质按F2、Cl2、Br2、I2顺序,下列性质递变规律正确的是( )
| A、颜色由浅变深 | B、氧化性逐渐增强 | C、氢化物的稳定性逐渐增强 | D、密度依次减小 |
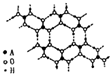 (2011?濮阳二模)A、B、C、D、E五种元素都是36号以前元素,原子序数依次增大,其相关信息如下表
(2011?濮阳二模)A、B、C、D、E五种元素都是36号以前元素,原子序数依次增大,其相关信息如下表