题目内容
【题目】“一碳化学”是指以含一个碳原子的化合物(如CO2、CO、CH4、CH3OH等)为初始反应物,合成一系列重要的化工原料和燃料的化学。
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应I:2NH3(g)+CO2(g)![]() NH2COONH4(s) H1
NH2COONH4(s) H1
反应II:NH2COONH4(s)![]() CO(NH2)2(s)+H2O(g) H2=+72.49kJ/mol
CO(NH2)2(s)+H2O(g) H2=+72.49kJ/mol
总反应:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g) H3=-86.98kJ/mol
CO(NH2)2(s)+H2O(g) H3=-86.98kJ/mol
请回答下列问题:
①反应I的H1=__kJ/mol。
②反应II一般在__(填“高温或“低温")条件下有利于该反应的进行。
③一定温度下,在体积固定的密闭容器中按计量比投料进行反应I,下列能说明反应达到了平衡状态的是__(填字母序号)。
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C.2v正(NH3)=v逆(CO2)
D.容器内混合气体的密度不再变化
(2)将CO2和H2按物质的量之比为1:3充入一定体积的密闭容器中,发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) H。测得CH3OH的物质的量在不同温度下随时间的变化关系如图所示。
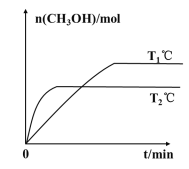
①根据图示判断H__0(填“>”或“<”)。
②一定温度下,在容积均为2L的两个密闭容器中,按如下方式加入反应物,10min后达到平衡。
容器 | 甲 | 乙 |
反应物投入量 | 1molCO2、3molH2 | amolCO2、bmolH2 cmolCH3OH(g)、cmolH2O(g)(a、b、c均不为零) |
若甲容器平衡后气体的压强为开始时的0.8倍,则反应10min内甲容器中以CH3OH(g)表示的化学反应速率为__,此温度下的化学平衡常数为__(保留两位小数);要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则乙容器中c的取值范围为__。
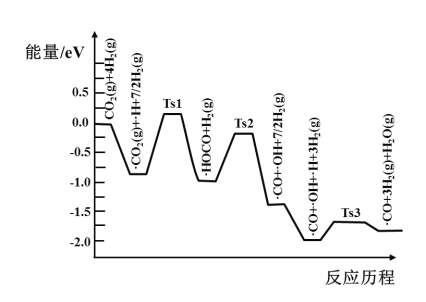
(3)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会__(填“放出热量”或“吸收热量”);反应历程中最小能垒(活化能)步骤的化学方程式为__。
CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会__(填“放出热量”或“吸收热量”);反应历程中最小能垒(活化能)步骤的化学方程式为__。
【答案】-159.47 高温 BD < 0.02mol·L-1·min-1 0.18 0.4<c<1 吸收热量 ![]() OH+
OH+![]() H== H2O(g)
H== H2O(g)
【解析】
(1)①根据盖斯定律计算反应I的H1;
②根据复合判据![]() 分析。
分析。
③根据平衡标志分析;
(2)①由图象可知,T2温度下反应速率快,所以T2>T1;升高温度,平衡时甲醇的物质的量减小;
②利用三段式计算反应速率和平衡常数;利用极值法判断c的取值范围;
(3)根据图象可知,吸附态的能量小于过渡态;活化能最小的过程是![]() CO、
CO、![]() OH、
OH、![]() H+3H2(g)生成
H+3H2(g)生成![]() CO+3H2(g)+H2O。
CO+3H2(g)+H2O。
(1)①反应I:2NH3(g)+CO2(g)![]() NH2COONH4(s) H1
NH2COONH4(s) H1
反应II:NH2COONH4(s)![]() CO(NH2)2(s)+H2O(g) H2=+72.49kJ/mol
CO(NH2)2(s)+H2O(g) H2=+72.49kJ/mol
根据盖斯定律I+II得总反应:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g) H3=-86.98kJ/mol,所以H1=-86.98kJ/mol-72.49kJ/mol=-159.47kJ/mol;
CO(NH2)2(s)+H2O(g) H3=-86.98kJ/mol,所以H1=-86.98kJ/mol-72.49kJ/mol=-159.47kJ/mol;
②NH2COONH4(s)![]() CO(NH2)2(s)+H2O(g) H>0,气体物质的量增大S>0,根据复合判据
CO(NH2)2(s)+H2O(g) H>0,气体物质的量增大S>0,根据复合判据![]() ,一般在高温条件下有利于该反应的进行;
,一般在高温条件下有利于该反应的进行;
③A.在体积固定的密闭容器中按计量比投料进行反应,容器中气体物质始终是NH3(g)、CO2且物质的量比等于2:1,所以混合气体的平均相对分子质量是定值,平均相对分子质量不再变化,不一定平衡,故不选A;
B.体积固定,正反应气体物质的量减小,所以压强是变量,容器内气体总压强不再变化,一定达到平衡状态,故选B;
C.反应达到平衡状态时,正逆反应的速率比等于系数比,v正(NH3)=2v逆(CO2)时达到平衡状态,2v正(NH3)=v逆(CO2)时反应没有达到平衡状态,故不选C;
D.体积固定,气体质量减小,密度是变量,若容器内混合气体的密度不再变化,一定达到平衡状态,故选D;
答案选BD;
(2)①由图象可知,T2温度下反应速率快,所以T2>T1;升高温度,平衡时甲醇的物质的量减小,即升高温度平衡逆向移动,H<0;
②设达到平衡是,CO2转化了xmol/L,根据三等式,有:
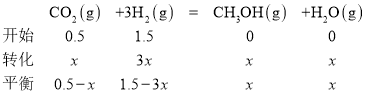
甲容器平衡后气体的压强为开始时的0.8倍,则![]() ,x=0.2;反应10min内甲容器中以CH3OH(g)表示的化学反应速率为
,x=0.2;反应10min内甲容器中以CH3OH(g)表示的化学反应速率为![]() 0.02mol·L-1·min-1,此温度下的化学平衡常数为
0.02mol·L-1·min-1,此温度下的化学平衡常数为![]() 0.18;
0.18;
平衡后乙容器与甲容器中相同组分的体积分数相等,说明甲乙的平衡是等效的。该反应CO2(g)+3H2(g)=CH3OH(g)+H2O(g)反应前后体积发生变化,在恒温恒容的条件下,两容器发生反应达到等效平衡,则“一边倒”后,加入的物质完全相同。若CO2和H2完全反应,则生成甲醇最大的量为1mol,达到平衡时,甲醇的物质的量为0.2mol/L×2=0.4mol,则乙容器中c的取值范围为0.4<c<1;
(3)根据图象可知,吸附态的能量小于过渡态,所以物质吸附在催化剂表面,形成过渡态的过程会吸收热量;活化能最小的过程是![]() CO、
CO、![]() OH、
OH、![]() H+3H2(g)生成
H+3H2(g)生成![]() CO+3H2(g)+H2O,反应方程式是
CO+3H2(g)+H2O,反应方程式是![]() OH+
OH+![]() H==H2O(g)。
H==H2O(g)。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案