题目内容
18. 已知H2O2的分子空间结构如图所示,H2O2分子不是直线形的,两个氢在犹如在半展开的书的两页上,氧原子则在书的夹缝上,书页夹角为93°,而两个O-H键与O-O键之间的夹角均为96°.有关H2O2结构的说法中正确的是( )
已知H2O2的分子空间结构如图所示,H2O2分子不是直线形的,两个氢在犹如在半展开的书的两页上,氧原子则在书的夹缝上,书页夹角为93°,而两个O-H键与O-O键之间的夹角均为96°.有关H2O2结构的说法中正确的是( )| A. | 分子的正、负电荷中心重合 | B. | 易溶于CS2 | ||
| C. | H2O2是极性分子 | D. | H2O2是非极性分子 |
分析 H2O2分子中,O-O键非极性键,而O-H键为极性键,结构不对称,正负电荷重心不重合,为极性分子,据此分析.
解答 解:A.分子结构不对称,正负电荷重心不重合,故A错误;
B.H2O2为极性分子,易溶于极性溶剂,难溶于非极性的CS2,故B错误;
C.分子结构不对称,正负电荷重心不重合,为极性分子,故C正确;
D.分子结构不对称,正负电荷重心不重合,为极性分子,故D错误.
故选C.
点评 本题考查了双氧水的结构和性质,侧重于共价键的考查,注意把握双氧水中键的极性和分子的极性,难度不大.

练习册系列答案
相关题目
8. 二氯化二硫(S2Cl2)在工业上用于橡胶的硫化,它极易与水反应.为在实验室合成S2Cl2,某化学研究性学习小组查阅有关资料,有如下两种反应原理:
二氯化二硫(S2Cl2)在工业上用于橡胶的硫化,它极易与水反应.为在实验室合成S2Cl2,某化学研究性学习小组查阅有关资料,有如下两种反应原理:
①CS2+3Cl2$\stackrel{95-100℃}{→}$CCl4+S2Cl2;②2S+Cl2$\stackrel{50-60℃}{→}$S2Cl2.
几种物质的熔、沸点数据如下表所示:
(1)如图装置(部分夹持仪器已略去)D到E有一处不够完善,清你提出改进的措施:在D、E之间再加一个干燥装置,同时要能吸收尾气、防倒吸;利用改进后的正确装置进行实验,反应原理应采用上述两个反应中的①(填①或②).
(2)B中盛放饱和氯化钠溶液,其作用是除去氯化氢;C中盛放试剂的名称是浓硫酸.
(3)D装置中水从冷凝管下端通入(选填“上”或“下”).反应结束后,从D装置锥形瓶内的混合物中分离出产品的操作为蒸馏(填名称).
(4)S2Cl2与水反应产生无色、有刺激性气味的气体,并有黄色沉淀生成,该反应的化学万程式为2S2Cl2+2H2O=S↓+SO2↑+4HCl.
 二氯化二硫(S2Cl2)在工业上用于橡胶的硫化,它极易与水反应.为在实验室合成S2Cl2,某化学研究性学习小组查阅有关资料,有如下两种反应原理:
二氯化二硫(S2Cl2)在工业上用于橡胶的硫化,它极易与水反应.为在实验室合成S2Cl2,某化学研究性学习小组查阅有关资料,有如下两种反应原理:①CS2+3Cl2$\stackrel{95-100℃}{→}$CCl4+S2Cl2;②2S+Cl2$\stackrel{50-60℃}{→}$S2Cl2.
几种物质的熔、沸点数据如下表所示:
| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | -109 | -23 | -77 |
(2)B中盛放饱和氯化钠溶液,其作用是除去氯化氢;C中盛放试剂的名称是浓硫酸.
(3)D装置中水从冷凝管下端通入(选填“上”或“下”).反应结束后,从D装置锥形瓶内的混合物中分离出产品的操作为蒸馏(填名称).
(4)S2Cl2与水反应产生无色、有刺激性气味的气体,并有黄色沉淀生成,该反应的化学万程式为2S2Cl2+2H2O=S↓+SO2↑+4HCl.
6.能正确表示下列反应的离子方程式是( )
| A. | 氯化钠与浓硫酸混合加热:H2SO4+2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$SO2↑+Cl2↑+H2O | |
| B. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH═2 Al(OH)3↓+3BaSO4↓ | |
| C. | Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
13.下列化合物的核磁共振氢谱中出现三组峰的是( )
| A. | 2,3一二甲基丁烷 | B. | 3-甲基-1-丁烯 | ||
| C. | 间二甲苯 | D. | 4,4-二甲基-1-戊炔 |
10.在一定条件下氯酸钾与碘按下式发生反应2KClO3+I2=2KIO3+Cl2由此可以推断下列相应结论不正确的是( )
| A. | 该反应属于置换反应 | B. | 还原性 I2>Cl2 | ||
| C. | 非金属性Cl>I | D. | 氧化性 I2>Cl2 |
7.短周期元素R,其原子的最外层比次外层少一个电子,则其氧化物的对应水化物的化学式不可能是( )
| A. | ROH | B. | H2RO4 | C. | HRO3 | D. | HRO4 |
8.下列说法正确的是( )
| A. | 常温下0.4 mol/L HB溶液和0.2 mol/L NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(B-)>c(H+)>c(Na+)>c(OH-) | |
| B. | 同浓度同体积的NaClO溶液和CH3COONa溶液,离子总数前者小于后者 | |
| C. | 在1mol/L CH3COOH溶液中加入少量冰醋酸,醋酸的电离平衡正向移动且电离程度增大 | |
| D. | 常温下0.1 mol/L的下列溶液①NH4Al(SO4)2;②NH4Cl;③NH3•H2O;④CH3COONH4中,c(NH4+)由大到小的顺序是:②>①>④>③ |
 .B与乙醇发生酯化反应生成X的化学方程式为
.B与乙醇发生酯化反应生成X的化学方程式为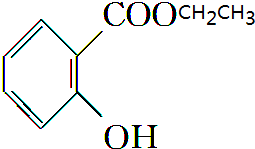 +H2O.
+H2O.
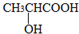 经过几步有机反应制得,其中最佳的次序是:a.
经过几步有机反应制得,其中最佳的次序是:a.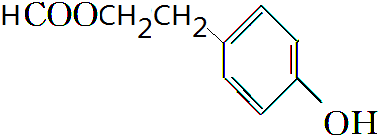
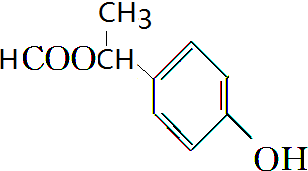 .
.