题目内容
3.镁、铝单质的化学性质以相似为主.但也存在某些重大差异性,下列物质能用于证明二者存在较大差异性的是( )①CO2;②盐酸;③Na0H溶液;④水.
| A. | ①④ | B. | ②③ | C. | ①③④ | D. | ②③④ |
分析 Mg是活泼金属与酸、水反应生成氢气,Mg与二氧化碳反应,Al为较活泼的金属与酸或强碱反应生成氢气,与水不反应,据此分析.
解答 解:①Mg与CO2反应生成MgO和碳,Al与CO2不反应,能用于证明二者存在较大差异性,故正确;
②盐酸与Mg、Al均能反应生成氢气,不能证明二者存在较大差异性,故错误;
③Mg与NaOH溶液不反应,Al与Na0H溶液反应生成氢气,能用于证明二者存在较大差异性,故正确;
④在热水中,镁与水会生成氢气,Al与热水不反应,能用于证明二者存在较大差异性,故正确;
所以①③④正确,
故选C.
点评 本题考查了金属镁和铝的性质,题目难度不大,注意把握Mg、Al性质想相似性和不同点,侧重于基础知识的考查.

练习册系列答案
相关题目
11.下列有关物质用途的叙述错误的是( )
| A. | 二氧化硅可制作光导纤维 | |
| B. | 因为氨易液化,在汽化时会吸收大量的热量,所以可作制冷剂 | |
| C. | 氧化钠在呼吸面具里作为氧气的来源 | |
| D. | 明矾可用作净水剂 |
18. 已知H2O2的分子空间结构如图所示,H2O2分子不是直线形的,两个氢在犹如在半展开的书的两页上,氧原子则在书的夹缝上,书页夹角为93°,而两个O-H键与O-O键之间的夹角均为96°.有关H2O2结构的说法中正确的是( )
已知H2O2的分子空间结构如图所示,H2O2分子不是直线形的,两个氢在犹如在半展开的书的两页上,氧原子则在书的夹缝上,书页夹角为93°,而两个O-H键与O-O键之间的夹角均为96°.有关H2O2结构的说法中正确的是( )
 已知H2O2的分子空间结构如图所示,H2O2分子不是直线形的,两个氢在犹如在半展开的书的两页上,氧原子则在书的夹缝上,书页夹角为93°,而两个O-H键与O-O键之间的夹角均为96°.有关H2O2结构的说法中正确的是( )
已知H2O2的分子空间结构如图所示,H2O2分子不是直线形的,两个氢在犹如在半展开的书的两页上,氧原子则在书的夹缝上,书页夹角为93°,而两个O-H键与O-O键之间的夹角均为96°.有关H2O2结构的说法中正确的是( )| A. | 分子的正、负电荷中心重合 | B. | 易溶于CS2 | ||
| C. | H2O2是极性分子 | D. | H2O2是非极性分子 |
8.下列各原子或离子的电子排列式错误的是( )
| A. | Na+ 1s22s22p6 | B. | F 1s22s22p6 | C. | N3+ 1s22s22p6 | D. | O2- 1s22s22p6 |


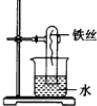
 Ⅰ.如图所示,在大试管里放入一段光亮无锈的弯成螺旋状的铁丝,把试管倒插入水中,把这个装置这样放置约一周后,观察到铁丝发生的变化是铁丝表面形成一层红棕色铁锈,原因是铁发生吸氧腐蚀.试管里的水面会上升,最终上升高度约为$\frac{1}{5}$,原因是O2约占空气的$\frac{1}{5}$,因正极发生反应O2+2H2O+4e-═4OH-,当O2消耗尽时,水上升高度约为$\frac{1}{5}$.
Ⅰ.如图所示,在大试管里放入一段光亮无锈的弯成螺旋状的铁丝,把试管倒插入水中,把这个装置这样放置约一周后,观察到铁丝发生的变化是铁丝表面形成一层红棕色铁锈,原因是铁发生吸氧腐蚀.试管里的水面会上升,最终上升高度约为$\frac{1}{5}$,原因是O2约占空气的$\frac{1}{5}$,因正极发生反应O2+2H2O+4e-═4OH-,当O2消耗尽时,水上升高度约为$\frac{1}{5}$.