题目内容
【题目】原电池的发明是化学对人类的一项重大贡献。
(1)一种新型燃料电池,它以多孔铂板为两个电极插入稀硫酸中,然后分别向两极通入氢气和氧气而获得电能。通入氢气的电极反应式为________________________。放电一段时间后,负极附近溶液的pH________(填“升高”“降低”或“不变”)。
(2)电子工业上常利用FeCl3溶液腐蚀铜板制作印刷电路,其反应的化学方程式为________________________。请把该反应设计成一个原电池,在方框内面出原电池装置图(要求:标明电极材料和电解质溶液)。_______

(3)常温下,将除去表面氧化膜的铝片、铜片插入浓HNO3中组成原电池装置如图甲所示,测得原电池的电流强度(I)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。
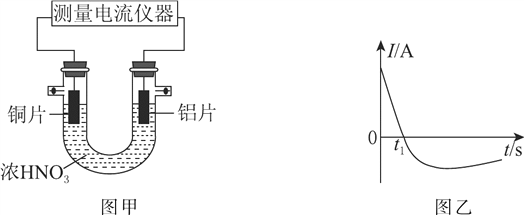
t1s前,原电池的负极是铝片,正极的电极反应式为____________,溶液中的H+向________(填“正”或“负”)极移动。t1s后,外电路中电子流动方向发生改变,其原因是________________________。
【答案】 H2-2e-=2H+ 降低 Cu+2FeCl3=CuCl2+2FeCl2 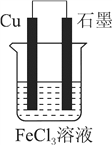 (需注明电解质溶液和电极名称,且构成闭合回路。) 2H++NO3-+e-=NO2↑+H2O 正 Al在浓硝酸中钝化,形成的氧化膜阻止了Al的进一步反应,此时Cu变成了负极
(需注明电解质溶液和电极名称,且构成闭合回路。) 2H++NO3-+e-=NO2↑+H2O 正 Al在浓硝酸中钝化,形成的氧化膜阻止了Al的进一步反应,此时Cu变成了负极
【解析】(1)由题意知,该燃料电池中,通入氢气的电极是负极,通入氧气的电极是正极,电解质是硫酸,所以通入氢气的电极反应式为H2-2e-=2H+。放电一段时间后,负极附近的氢离子浓度变大,溶液的pH降低。
(2)电子工业上常利用FeCl3溶液腐蚀铜板制作印刷电路,其反应的化学方程式为Cu+2FeCl3=CuCl2+2FeCl2。把该反应设计成一个原电池,还原剂铜必须做负极,正极要用没有铜活泼的材料,电解质溶液一定是氯化铁溶液,原电池装置图如下:
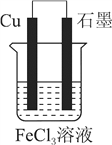
(3)由图像可知,在t1s前后,电路中的电流方向是相反的,所以t1s前,因为铝比铜活泼,原电池的负极是铝片,铝发生氧化反应生成氧化铝,正极为铜,正极上硝酸根被还原为二氧化氮,正极的电极反应式为2H++NO3-+e-=NO2↑+H2O,溶液中的H+向正极移动。当铝表面被全部氧化生成致密的氧化膜后,铝电极不如铜活泼,所以t1s后,,外电路中电子流动方向发生改变,其原因是Al在浓硝酸中钝化,形成的氧化膜阻止了Al的进一步反应,此时Cu变成了负极。

【题目】如表列出了①~⑥六种元素在元素周期表中的位置.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ |
请回答下列问题:
(1)①、②、③三种元素相比较,非金属性最强的是 (填写元素符号);
(2)元素①③⑥的氢化物的分子式分别是 ; ; .
(3)④、⑤两种元素的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是 .
【题目】I.配制250mL0.5mol/L的NaOH溶液,所需的仪器有烧杯、玻璃棒、托盘天平、胶头滴管和_______。定容时俯视观察刻度线,其结果_______。(填“偏大”、“偏小”、或“不变”)
Ⅱ.实验室用加热固体氯化铵和氢氧化钙的混合物制取氨气,反应的化学方程式是_______;所制得的气体中常含有少量杂质气体,为了得到纯净的氨气并加以检验,请在下列装置或试剂中,根据要求作出合适选择,并将对应选择的装置编号字母填入表中的空格处:
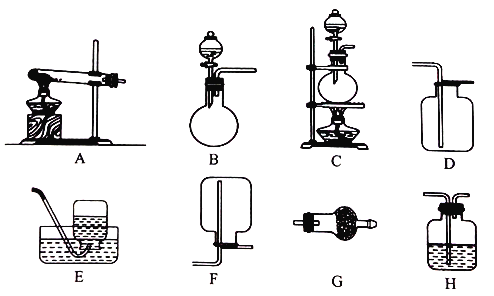
试剂:a. NaOH溶液 b.澄清石灰水 c.浓硫酸 d.饱和NaHCO3溶液 e.碱石灰
f.品红溶液 g.湿润的红色石蕊试纸
制取气体 | 杂质气体 | 制取气体的 发生装置 | 收集装置 | 净化装置中 所用的试剂 | 检验制得的气体 所用试剂 |
NH3 | H2O(g) | _______ | F | e | _______ |
【题目】1,2-二溴乙烷可作抗爆剂的添加剂。如图为实验室制备1,2-二溴乙烷的装罝图, 图中分液制斗和烧瓶a中分别装有浓H2SO4和无水乙醇,d装罝试管中装有液溴。

己知:CH3CH2OH![]() CH2=CH2↑+H2O;2CH3CH2OH
CH2=CH2↑+H2O;2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
相关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
状态 | 无色液体 | 无色液体 | 无色液体 | 红棕色液体 |
密度/g·cm-3 | 0.79 | 2.18 | 0.71 | 3.10 |
沸点/℃ | 78.5 | 131.4 | 34.6 | 58.8 |
熔点/℃ | -114.3 | 9.79 | - 116.2 | -7.2 |
水溶性 | 混溶 | 难溶 | 微溶 | 可溶 |
(1)实验中应迅速将温度升卨到170℃左右的原因是______________________________。
(2)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装罝中导管是否发生堵塞,
请写出发生堵塞时瓶b中的现象:①_______________________________;如果实验时d装罝中导管堵塞,你认为可能的原因是②_______________________________________________;安全瓶b还可以起到的作用是③__________________。
(3)容器c、e中都盛有NaOH溶液,c中NaOH溶液的作用是_______________________________。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正确情况下超过许多,如果装罝的气密性没有问题,试分析可能的原因:______________、______________(写出两条即可)。
(5)除去产物中少量未反应的Br2后,还含有的主要杂质为___________,要进一步提纯,下列操作中必需的是_____________ (填字母)。
A.重结晶 B.过滤 C.萃取 D.蒸馏
(6)实验中也可以撤去d装罝中盛冰水的烧杯,改为将冷水直接加入到d装罝的试管中,则 此时冷水除了能起到冷却1,2-二溴乙烷的作用外,还可以起到的作用是____________________________。