题目内容
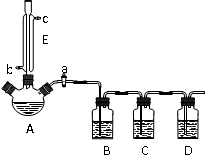
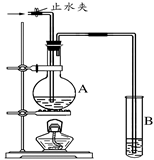
(16分)制备溴苯的实验装置如右图所示,回答下列问题:

(1)该反应装置中仪器A的名称为 。反应开始前已向仪器A中加入的固体药品是铁粉,而装在左侧分液漏斗中的液体药品是 。
(2)冷凝管B有上、下两口,冷却水应从 口进入
(3)导管口不能插入锥形瓶中的液面之下,其原因 是 ;
(4)右侧分液漏斗中的物质在反应 时加入A中(填写反应前、反应中或者反应后)。用离子方程式表达其作用是 。
(5)反应结束向锥形瓶中的液体中加入硝酸酸化的硝酸银溶液,可见到现象是 。
(6)该过程可以如下表述:3Br2+2Fe=2FeBr3;Br2+FeBr3=FeBr4-+Br+(不稳定);
 +Br+→[
+Br+→[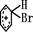 ];[
];[ ]+FeBr4-→
]+FeBr4-→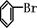 +HBr+FeBr3;
+HBr+FeBr3;
由上反应可知: +Br2→
+Br2→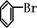 +HBr中的催化剂为( )
+HBr中的催化剂为( )
A Fe B FeBr3 C Br+ D FeBr4-

(1)该反应装置中仪器A的名称为 。反应开始前已向仪器A中加入的固体药品是铁粉,而装在左侧分液漏斗中的液体药品是 。
(2)冷凝管B有上、下两口,冷却水应从 口进入
(3)导管口不能插入锥形瓶中的液面之下,其原因 是 ;
(4)右侧分液漏斗中的物质在反应 时加入A中(填写反应前、反应中或者反应后)。用离子方程式表达其作用是 。
(5)反应结束向锥形瓶中的液体中加入硝酸酸化的硝酸银溶液,可见到现象是 。
(6)该过程可以如下表述:3Br2+2Fe=2FeBr3;Br2+FeBr3=FeBr4-+Br+(不稳定);
 +Br+→[
+Br+→[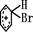 ];[
];[ ]+FeBr4-→
]+FeBr4-→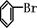 +HBr+FeBr3;
+HBr+FeBr3;由上反应可知:
 +Br2→
+Br2→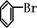 +HBr中的催化剂为( )
+HBr中的催化剂为( )A Fe B FeBr3 C Br+ D FeBr4-
(16分)
(1)三颈烧瓶;苯、液溴
(2)下口
(3)防止倒吸
(4)反应后;Br2+2OH-=Br-+BrO-+ H2O
(5)浅黄色沉淀
(6)B
(1)三颈烧瓶;苯、液溴
(2)下口
(3)防止倒吸
(4)反应后;Br2+2OH-=Br-+BrO-+ H2O
(5)浅黄色沉淀
(6)B
(1)由反应原理 +Br2→
+Br2→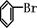 +HBr可知,在三颈烧瓶中放有铁粉,左边的分液漏斗盛放反应液苯及液溴,右边的分液漏斗中盛放碱液,中间的出口起得作用为:导出HBr气体及冷凝反应液
+HBr可知,在三颈烧瓶中放有铁粉,左边的分液漏斗盛放反应液苯及液溴,右边的分液漏斗中盛放碱液,中间的出口起得作用为:导出HBr气体及冷凝反应液
(2)冷凝管冷水入口为下口,保证热蒸气始终遇到的是冷水
(3)HBr极易溶于水,易形成倒吸,故导管下端不应插入液面下
(4)反应后,由于未反应的溴与生成物溴苯混合在一起,为除去溴,可将NaOH溶液注入三颈烧瓶中:Br2+2OH-=Br-+BrO-+ H2O
(5)生成的HBr及部分溴会进入锥形瓶中,如果加入硝酸酸化的硝酸银溶液,可得到AgBr浅黄色沉淀
(6)从反应机理可看出,FeBr3在反应中的量并没有改变,属于催化剂,而Br+、FeBr4-均为中间产物
 +Br2→
+Br2→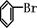 +HBr可知,在三颈烧瓶中放有铁粉,左边的分液漏斗盛放反应液苯及液溴,右边的分液漏斗中盛放碱液,中间的出口起得作用为:导出HBr气体及冷凝反应液
+HBr可知,在三颈烧瓶中放有铁粉,左边的分液漏斗盛放反应液苯及液溴,右边的分液漏斗中盛放碱液,中间的出口起得作用为:导出HBr气体及冷凝反应液(2)冷凝管冷水入口为下口,保证热蒸气始终遇到的是冷水
(3)HBr极易溶于水,易形成倒吸,故导管下端不应插入液面下
(4)反应后,由于未反应的溴与生成物溴苯混合在一起,为除去溴,可将NaOH溶液注入三颈烧瓶中:Br2+2OH-=Br-+BrO-+ H2O
(5)生成的HBr及部分溴会进入锥形瓶中,如果加入硝酸酸化的硝酸银溶液,可得到AgBr浅黄色沉淀
(6)从反应机理可看出,FeBr3在反应中的量并没有改变,属于催化剂,而Br+、FeBr4-均为中间产物

练习册系列答案
相关题目

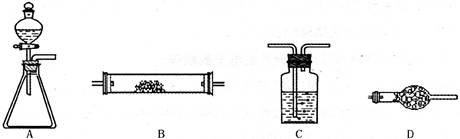
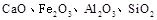 组成,由榴石矿石制取氯化钙和氧化铝的实验步骤如下:
组成,由榴石矿石制取氯化钙和氧化铝的实验步骤如下: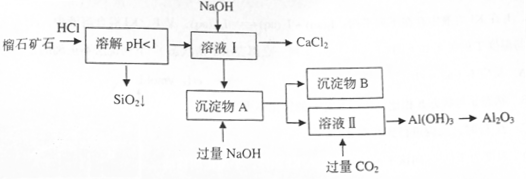
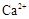 外,还含有的金属离子是 。
外,还含有的金属离子是 。
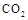 气体并通入溶液II中,结果没有沉淀产生,可能的原是 ;为了能产生沉淀该同学对图I装置进行了改进,改进的方法为 。
气体并通入溶液II中,结果没有沉淀产生,可能的原是 ;为了能产生沉淀该同学对图I装置进行了改进,改进的方法为 。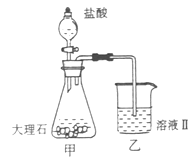
 .3
.3