题目内容
(14分)下图所示是用于气体制备、干燥(或除杂质)、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去,各装置可重复使用也可不用)。请根据下列要求回答问题。
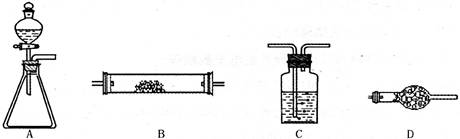
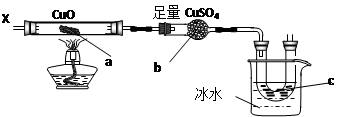
(1)若用A-C-D-B组合进行氢气还原氧化铜实验。分液漏斗中的试剂是盐酸,C中试剂是水,其作用是 ;A中反应开始后,加热B之前的实验操作是 ,加热后B中将观察到的现象是 。B中反应的化学方程式 。
(2)为验证氯气不能使干燥的红布条褪色,置红布条于B中,按A-C-B-D连接成实验装置体系。A锥形瓶中试剂选用高锰酸钾晶体,则分液漏斗中的液体是 ;C中试剂是 ,D的作用是 。
(3)为了进行氨的催化氧化实验,若锥形瓶中盛装足量的Na2O2粉末,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,产生的气体通过红热的铂粉,各仪器装置按气流方向从左到右连接顺序是(填字母) ;装置B中可能发生反应的化学方程式为: 。

(1)若用A-C-D-B组合进行氢气还原氧化铜实验。分液漏斗中的试剂是盐酸,C中试剂是水,其作用是 ;A中反应开始后,加热B之前的实验操作是 ,加热后B中将观察到的现象是 。B中反应的化学方程式 。
(2)为验证氯气不能使干燥的红布条褪色,置红布条于B中,按A-C-B-D连接成实验装置体系。A锥形瓶中试剂选用高锰酸钾晶体,则分液漏斗中的液体是 ;C中试剂是 ,D的作用是 。
(3)为了进行氨的催化氧化实验,若锥形瓶中盛装足量的Na2O2粉末,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,产生的气体通过红热的铂粉,各仪器装置按气流方向从左到右连接顺序是(填字母) ;装置B中可能发生反应的化学方程式为: 。
(14分)
(1)吸收氢气中的HCl(1分)(填“除去HCl”等合理答案可得分,填“除杂”不得分。) 检验氢气纯度(1分)(填“验纯H2”等合理答案可得分) 固体粉末由黑变红(2分)(填“固体变红”等合理答案可得分) H2+CuO Cu+H2O(2分)(化学式写错、未配平均不得分。条件漏写扣1分。)
Cu+H2O(2分)(化学式写错、未配平均不得分。条件漏写扣1分。)
(2)浓盐酸(1分)(填“盐酸”可得分) 浓硫酸(1分) 吸收氯气以免污染环境(2分)(填“除去氯气”等合理答案可得分。)
(3)ADBD(D盛装碱石灰)或ADBC(C盛装氢氧化钠溶液) (2分);
4NH3+5O2 4NO+6H2O(2分)(化学式写错、未正确配平不得分,条件漏写扣1分,多写“2NO+O2=2NO2”不扣分)
4NO+6H2O(2分)(化学式写错、未正确配平不得分,条件漏写扣1分,多写“2NO+O2=2NO2”不扣分)
(1)吸收氢气中的HCl(1分)(填“除去HCl”等合理答案可得分,填“除杂”不得分。) 检验氢气纯度(1分)(填“验纯H2”等合理答案可得分) 固体粉末由黑变红(2分)(填“固体变红”等合理答案可得分) H2+CuO
 Cu+H2O(2分)(化学式写错、未配平均不得分。条件漏写扣1分。)
Cu+H2O(2分)(化学式写错、未配平均不得分。条件漏写扣1分。)(2)浓盐酸(1分)(填“盐酸”可得分) 浓硫酸(1分) 吸收氯气以免污染环境(2分)(填“除去氯气”等合理答案可得分。)
(3)ADBD(D盛装碱石灰)或ADBC(C盛装氢氧化钠溶液) (2分);
4NH3+5O2
 4NO+6H2O(2分)(化学式写错、未正确配平不得分,条件漏写扣1分,多写“2NO+O2=2NO2”不扣分)
4NO+6H2O(2分)(化学式写错、未正确配平不得分,条件漏写扣1分,多写“2NO+O2=2NO2”不扣分)考查气体的制取、净化及性质
(1)氢气还原氧化铜:H2+CuO Cu+H2O,很明显CD装置均为除杂装置,由于盐酸易挥发,故氢气中有两种气体杂质:水蒸气及HCl;故用水来吸收HCl,再用干燥管D来干燥氢气,进而还原CuO
Cu+H2O,很明显CD装置均为除杂装置,由于盐酸易挥发,故氢气中有两种气体杂质:水蒸气及HCl;故用水来吸收HCl,再用干燥管D来干燥氢气,进而还原CuO
由于氢气可燃,故在还原之前必须验纯;
黑色的氧化铜粉末被还原为黑色的金属铜
(2)常温下高锰酸钾可将浓盐酸氧化为氯气:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O;
而C瓶中可装浓硫酸以干燥氯气;B管中分别放置干燥、湿润的有色布条;D中可加入碱石灰,以吸收氯气,防止污染空气
(3)Na2O2粉末与水生成氧气:2Na2O2+2H2O=4NaOH+O2↑,混合气体氨气及氧气经D装置干燥后进入B管中进行催化氧化:4NH3+5O2 4NO+6H2O,最后再用碱液吸收NO或NO2等有毒气体,故装置的连接顺序为ADBC
4NO+6H2O,最后再用碱液吸收NO或NO2等有毒气体,故装置的连接顺序为ADBC
(1)氢气还原氧化铜:H2+CuO
 Cu+H2O,很明显CD装置均为除杂装置,由于盐酸易挥发,故氢气中有两种气体杂质:水蒸气及HCl;故用水来吸收HCl,再用干燥管D来干燥氢气,进而还原CuO
Cu+H2O,很明显CD装置均为除杂装置,由于盐酸易挥发,故氢气中有两种气体杂质:水蒸气及HCl;故用水来吸收HCl,再用干燥管D来干燥氢气,进而还原CuO由于氢气可燃,故在还原之前必须验纯;
黑色的氧化铜粉末被还原为黑色的金属铜
(2)常温下高锰酸钾可将浓盐酸氧化为氯气:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O;
而C瓶中可装浓硫酸以干燥氯气;B管中分别放置干燥、湿润的有色布条;D中可加入碱石灰,以吸收氯气,防止污染空气
(3)Na2O2粉末与水生成氧气:2Na2O2+2H2O=4NaOH+O2↑,混合气体氨气及氧气经D装置干燥后进入B管中进行催化氧化:4NH3+5O2
 4NO+6H2O,最后再用碱液吸收NO或NO2等有毒气体,故装置的连接顺序为ADBC
4NO+6H2O,最后再用碱液吸收NO或NO2等有毒气体,故装置的连接顺序为ADBC
练习册系列答案
相关题目
 3Cu+3H2O+N2,纯氮气跟镁在高温下反应可得到氮化镁,但氮化镁遇水即剧烈反应生成氢氧化镁和氨气。下面是某化学课外小组的同学提出的实验室制备氨气的几种方案:
3Cu+3H2O+N2,纯氮气跟镁在高温下反应可得到氮化镁,但氮化镁遇水即剧烈反应生成氢氧化镁和氨气。下面是某化学课外小组的同学提出的实验室制备氨气的几种方案: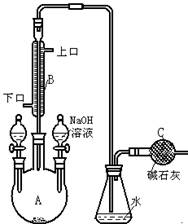
 +Br+→[
+Br+→[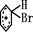 ];[
];[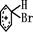 ]+FeBr4-→
]+FeBr4-→ +HBr+FeBr3;
+HBr+FeBr3; +Br2→
+Br2→ +HBr中的催化剂为( )
+HBr中的催化剂为( )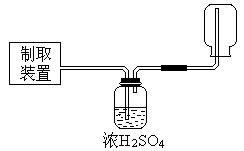

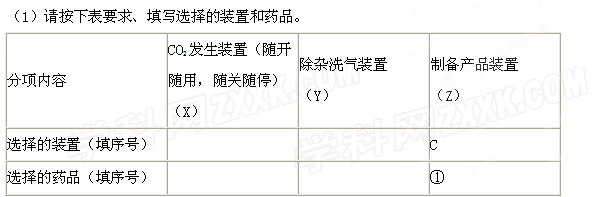
 过量CO2后,Z装置内的溶液中离子浓度大小顺序为 ;若要保证乙装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过 %(质量分数)。
过量CO2后,Z装置内的溶液中离子浓度大小顺序为 ;若要保证乙装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过 %(质量分数)。