题目内容
14.(10分)根据要求回答下列问题:①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧Al
(1)只含有离子键的是(用序号回答,下同)①
(2)含有共价键的离子化合物是③⑤⑥
(3)属于共价化合物的是②④⑦
(4)熔融状态能导电的化合物是①③⑤⑥
(5)熔融状态时和固态时,都能导电的是⑧.
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,碱金属族、碱土金属族元素和氧族、卤族元素之间易形成离子键,
(1)溴化钙中只含离子键;
(2)离子化合物中一定含有离子键,可能含有共价键;
(3)只含共价键的化合物是共价化合物;
(4)离子化合物是在熔融状态下能导电的化合物;
(5)金属单质在固体和熔融状态下都能导电.
解答 解:活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,碱金属族、碱土金属族元素和氧族、卤族元素之间易形成离子键,
(1)溴化钙中只含离子键,故选①;
(2)离子化合物中一定含有离子键,可能含有共价键,含有共价键的离子化合物是③⑤⑥,故选③⑤⑥;
(3)只含共价键的化合物是共价化合物,只含共价键的化合物是②④⑦,故选②④⑦;
(4)离子化合物是在熔融状态下能导电的化合物,熔融状态下能导电的化合物是①③⑤⑥;
(5)金属单质在固体和熔融状态下都能导电,只有Al在固态和熔融状态下能导电,故选⑧.
点评 本题考查化合物类型及物质的导电性等知识点,侧重考查分析判断能力及基本概念,明确物质的构成微粒是解本题关键,可以根据熔融状态下是否导电判断离子化合物和共价化合物.

练习册系列答案
相关题目
5.m mol乙炔跟n mol氢气在密闭容器中反应,当其达到平衡时生成p mol乙烯,将平衡混合气体完全燃烧生成CO2和H2O,所需氧气的物质的量是( )
| A. | (3m+n)mol | B. | (3m+n+2p)mol | C. | (2.5m+0.5n-3p)mol | D. | (2.5m+0.5n)mol |
2.下列离子方程式中书写正确的是( )
| A. | 铝粉与烧碱溶液反应:Al+6OH+═[Al(OH)4]-+H2↑ | |
| B. | 水玻璃中加入稀盐酸:Na2SiO4+2H+═H2SiO3↓+2Na+ | |
| C. | 二氧化硅与苛性钠溶液反应:SiO2+2OH-═SiO32-+H2O | |
| D. | 将氯气通入到水中:Cl2+H2O═2HCl-+ClO- |
9.下列有机反应的方程式书写错误的是( )
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | B. | CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH | ||
| C. |  +HNO3$→_{50-60℃}^{浓硫酸}$ +HNO3$→_{50-60℃}^{浓硫酸}$ +H2O +H2O | D. | nCH2=CH2$\stackrel{一定条件}{→}$ |
3.配制一定物质的量浓度的KOH溶液时,导致所配溶液浓度偏低的原因可能是( )
| A. | 定容时俯视 | B. | 容量瓶中原有少量的蒸馏水 | ||
| C. | 容量瓶盛过KOH溶液,使用前未洗涤 | D. | 转移时,不慎将液体流到瓶外 |
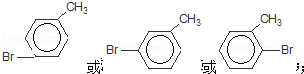
4.下列物质与NaOH醇溶液共热完全反应后,可得3种有机物的是( )
| A. | CH3-CHCl-CH2-CH3 | B. | 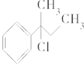 | ||
| C. | CH3-C(CH3)Cl-CH2-CH3 | D. | 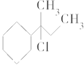 |
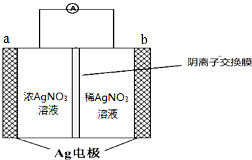 银是一种在工业、生活上有广泛用途的金属.
银是一种在工业、生活上有广泛用途的金属.