题目内容
(14分)合成氨是人类研究的重要课题,目前工业合成氨的原理为:
合成氨是人类研究的重要课题,目前工业合成氨的原理为:
N2(g)+3H2(g) 2NH3(g)△H=-93.0kJ?mol-1,在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:
2NH3(g)△H=-93.0kJ?mol-1,在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:
相持恒温、恒容,测的反应达到平衡时关系数据如下:
(1)下列各项能说明该反应已到达平衡状态的是 (填写序号字母)
a.容器内H2、N2、NH3的浓度只比为1:3:2 b.容器内压强保持不变
c.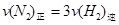 d.混合气体的密度保持不变
d.混合气体的密度保持不变
e.混合气体的平均相对分子质量不变
(2)容器乙中反应从开始到达平衡的反应速度为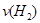 =
=
(3)在该温度下甲容器中反应的平衡常数K (用含C1的代数式表示)
(4)分析上表数据,下列关系正确的是 (填序号):
a.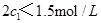 b.氮气的转化率:
b.氮气的转化率: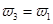 c.
c. 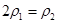 d.
d.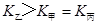
(5)另据报道,常温、常压下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成NH3和O2。已知:H2的燃烧热△H=-286KJ/mol,则由次原理制NH3反应的热化学方程式为
(6)希腊阿里斯多德大学的George Mamellos和Michacl Stoukides,发明了一种合成氨的新方法,在常压下,把氢气和用氨气稀释的氮气分别通入一个加热到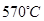 的电解池,李勇能通过的氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,在电解法合成氨的过程中,应将N2不断地通入 极,该电极反应式为 。
的电解池,李勇能通过的氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,在电解法合成氨的过程中,应将N2不断地通入 极,该电极反应式为 。
合成氨是人类研究的重要课题,目前工业合成氨的原理为:
N2(g)+3H2(g)
 2NH3(g)△H=-93.0kJ?mol-1,在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:
2NH3(g)△H=-93.0kJ?mol-1,在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:相持恒温、恒容,测的反应达到平衡时关系数据如下:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3molH2、2molN2 | 6molH2、4molN2 | 2mol NH3 |
| 达到平衡的时间/min | | 6 | 8 |
| 平衡时 N2的体积密度 | C1 | 1.5 | |
| 混合气体密度/g·L-1 | 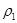 | 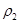 | |
| 平衡常数/ L2·mol-2 | K甲 | K乙 | K丙 |
a.容器内H2、N2、NH3的浓度只比为1:3:2 b.容器内压强保持不变
c.
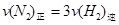 d.混合气体的密度保持不变
d.混合气体的密度保持不变e.混合气体的平均相对分子质量不变
(2)容器乙中反应从开始到达平衡的反应速度为
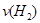 =
= (3)在该温度下甲容器中反应的平衡常数K (用含C1的代数式表示)
(4)分析上表数据,下列关系正确的是 (填序号):
a.
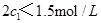 b.氮气的转化率:
b.氮气的转化率: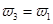 c.
c. 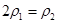 d.
d.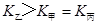
(5)另据报道,常温、常压下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成NH3和O2。已知:H2的燃烧热△H=-286KJ/mol,则由次原理制NH3反应的热化学方程式为
(6)希腊阿里斯多德大学的George Mamellos和Michacl Stoukides,发明了一种合成氨的新方法,在常压下,把氢气和用氨气稀释的氮气分别通入一个加热到
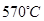 的电解池,李勇能通过的氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,在电解法合成氨的过程中,应将N2不断地通入 极,该电极反应式为 。
的电解池,李勇能通过的氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,在电解法合成氨的过程中,应将N2不断地通入 极,该电极反应式为 。(14分,每空2分)(1)be(全对2分,对1个得1分,有错不得分)
(2)0.25mol/(L·min)(单位不写或错写扣1分)
(3)K=4(1-C1)2/C1·(3C1-1.5)3
(4)C
(5)2N2(g)+6H2O(l)="4" NH3(g)+3 O2(g)△H=+1530kJ·mol-1
(6)阴 N2+6H+++6e-==2 NH3
(2)0.25mol/(L·min)(单位不写或错写扣1分)
(3)K=4(1-C1)2/C1·(3C1-1.5)3
(4)C
(5)2N2(g)+6H2O(l)="4" NH3(g)+3 O2(g)△H=+1530kJ·mol-1
(6)阴 N2+6H+++6e-==2 NH3
试题分析:(1)合成氨反应是反应前后气体物质的量发生变化的可逆反应,所以压强不变时证明已达平衡状态,b正确;容器内的各物质的浓度比符合化学计量数之比时未必是平衡状态,a错误;根据好好的定义,正逆反应速率相等时达平衡状态,氢气的反应速率是氮气反应速率的3倍,c错误;容器的体积不变,所以气体的密度始终不变,d错误;气体的质量不变,而气体的总物质的量变化,当平均相对分子质量不变时已达平衡状态,e正确,答案选be;
(2)根据氮气的体积密度即浓度可计算平衡时氮气的物质的量为3mol,则消耗氮气的物质的量是1mol,氢气的物质的量是3mol,所以用氢气表示的反应速率为3mol/2L/6min="0.25" mol/(L·min);
(3)氮气、氢气的起始浓度分别为1mol/L、1.5mol/L,根据氮气平衡时的浓度可计算消耗氮气的浓度为1- C1,消耗氢气的浓度是3(1- C1),生成氨气的浓度为2(1- C1),根据化学平衡常数的表达式可得K甲=c(NH3)2/c(N2)c(H2)3=4(1-C1)2/C1·(3C1-1.5)3
(4)A、乙容器的反应物浓度是甲容器的2倍,保持恒温、恒容,乙容器相当于在2个甲的基础上又正向移动,氮气的浓度减小,所以2 C1>1.5mol/L,错误;B、把丙的2mol氨气转化为3mol氢气和1mol氮气与丙达到的平衡是等效的。甲与丙相比,甲的氢气浓度大,氮气的转化率高,错误;C、乙容器的气体质量是甲容器的气体质量的2倍,容器的体积都为2L,所以
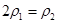 ,正确;D、三个容器的温度相同,则化学平衡常数相等,错误,答案选C;
,正确;D、三个容器的温度相同,则化学平衡常数相等,错误,答案选C;(5)根据盖斯定律N2(g)+3H2(g)=2NH3(g)△H=-93.0kJ?mol-1,①
2 H2(g)+O2(g)="2" H2O(l) △H="-572" kJ?mol-1 ②
则2N2(g)+6H2O(l)="4" NH3(g)+3 O2(g)的△H=①×2-②×3="+1530" kJ?mol-,所以所求热化学方程式为
2N2(g)+6H2O(l)="4" NH3(g)+3 O2(g)△H=+1530kJ·mol-1
(6)氮气中的N元素化合价为0,氨气中的N元素的化合价为-3,所以氮气发生还原反应,则氮气是电解池的阴极;发生的电极反应式为N2+6H+++6e-==2 NH3

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 CH3OH(g);△H=-dJ·mol-1(d>0)。初始投料与各容器达到平衡时的有关数据如下:
CH3OH(g);△H=-dJ·mol-1(d>0)。初始投料与各容器达到平衡时的有关数据如下:
 N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是 。
N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是 。

 O2(g)=H2O(g) △H=-241.8kJ·mol-1
O2(g)=H2O(g) △H=-241.8kJ·mol-1 2NO(g) △H
2NO(g) △H 0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在2.0 L密闭汽缸内经过5s反应达到平衡,测得NO为1.6×10-3mol。
0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在2.0 L密闭汽缸内经过5s反应达到平衡,测得NO为1.6×10-3mol。  2CO2(g)+N2(g) 中,NO的浓度c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2(g)+N2(g) 中,NO的浓度c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。

 3AlCl(g)+3CO(g) ΔH="a" kJ·mol-1
3AlCl(g)+3CO(g) ΔH="a" kJ·mol-1