题目内容
对大气污染物SO2、NOx进行研究具有重要环保意义。请回答下列问题:
(1)为减少SO2的排放,常采取的措施是将煤转化为清洁气体燃料。
已知:① H2(g)+ O2(g)=H2O(g) △H=-241.8kJ·mol-1
O2(g)=H2O(g) △H=-241.8kJ·mol-1
②C(s)+ O2(g)=CO(g) △H=-110.5kJ·mol-1
O2(g)=CO(g) △H=-110.5kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式: 。
(2)已知汽车汽缸中生成NO的反应为:N2(g)+O2(g) 2NO(g) △H
2NO(g) △H 0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在2.0 L密闭汽缸内经过5s反应达到平衡,测得NO为1.6×10-3mol。
0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在2.0 L密闭汽缸内经过5s反应达到平衡,测得NO为1.6×10-3mol。
①在1300oC 时,该反应的平衡常数表达式K= 。5s内该反应的平均速率ν(N2) = (保留2位有效数字);
②汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是 。
(3)汽车尾气中NO和CO的转化。当催化剂质量一定时,增大催化剂固体的表面积可提高化学反应速率。下图表示在其他条件不变时,反应2NO(g)+2CO(g) 2CO2(g)+N2(g) 中,NO的浓度c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2(g)+N2(g) 中,NO的浓度c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。

①该反应的△H 0 (填“>”或“<”)。
②若催化剂的表面积S1>S2,在右图中画出c(NO) 在T1、S2条件下达到平衡过程中的变化曲线(并作相应标注)。
(1)为减少SO2的排放,常采取的措施是将煤转化为清洁气体燃料。
已知:① H2(g)+
 O2(g)=H2O(g) △H=-241.8kJ·mol-1
O2(g)=H2O(g) △H=-241.8kJ·mol-1②C(s)+
 O2(g)=CO(g) △H=-110.5kJ·mol-1
O2(g)=CO(g) △H=-110.5kJ·mol-1写出焦炭与水蒸气反应的热化学方程式: 。
(2)已知汽车汽缸中生成NO的反应为:N2(g)+O2(g)
 2NO(g) △H
2NO(g) △H 0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在2.0 L密闭汽缸内经过5s反应达到平衡,测得NO为1.6×10-3mol。
0,若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在2.0 L密闭汽缸内经过5s反应达到平衡,测得NO为1.6×10-3mol。 ①在1300oC 时,该反应的平衡常数表达式K= 。5s内该反应的平均速率ν(N2) = (保留2位有效数字);
②汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是 。
(3)汽车尾气中NO和CO的转化。当催化剂质量一定时,增大催化剂固体的表面积可提高化学反应速率。下图表示在其他条件不变时,反应2NO(g)+2CO(g)
 2CO2(g)+N2(g) 中,NO的浓度c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2(g)+N2(g) 中,NO的浓度c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
①该反应的△H 0 (填“>”或“<”)。
②若催化剂的表面积S1>S2,在右图中画出c(NO) 在T1、S2条件下达到平衡过程中的变化曲线(并作相应标注)。
(1)C(s) + H2O(g) =" CO(g)" + H2(g) △H=+131.3kJ·mol-1
(2)①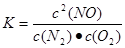 8.0×10-5 mol/(L·s)。
8.0×10-5 mol/(L·s)。
② 温度升高,反应速度加快,平衡向右移动(3)① <
②见右图: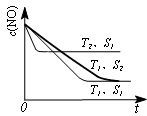
(2)①
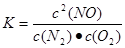 8.0×10-5 mol/(L·s)。
8.0×10-5 mol/(L·s)。② 温度升高,反应速度加快,平衡向右移动(3)① <
②见右图:

试题分析:(1)②-①整理可得:C(s) + H2O(g) =" CO(g)" + H2(g) △H=+131.3kJ/mol。(2)①N2(g)+O2(g)
 2NO(g)的化学平衡常数为
2NO(g)的化学平衡常数为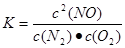 经过5s反应达到平衡时,测得NO为1.6×10-3mol
经过5s反应达到平衡时,测得NO为1.6×10-3mol,根据化学方程式物质间的关系可知消耗N2的物质的量为8.0×10-3mol.则V(N2)= 8.0×10-4mol÷2.0 L÷5s=8.0×10-5 mol/(L·s)。②由于化学反应N2(g)+O2(g)
 2NO(g) 的正反应是吸热反应,汽车启动后,汽缸温度越高,化学反应速率加快。根据平衡移动原理,升高温度,化学平衡正向移动,会产生更多的NO。所以单位时间内NO排放量越大。(3)由图像可知在温度为T2时先达到平衡。说明温度T2>T1。①由于温度升高,NO的浓度增大。根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。逆反应方向为吸热反应,所以该反应的正反应为放热反应△H<0.②若催化剂的表面积S1>S2。在其它条件不变时,催化剂的表面积越大,反应速率越快,达到平衡所需要的时间就越短。在T1、S2条件下达到平衡过程中的变化曲线为
2NO(g) 的正反应是吸热反应,汽车启动后,汽缸温度越高,化学反应速率加快。根据平衡移动原理,升高温度,化学平衡正向移动,会产生更多的NO。所以单位时间内NO排放量越大。(3)由图像可知在温度为T2时先达到平衡。说明温度T2>T1。①由于温度升高,NO的浓度增大。根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。逆反应方向为吸热反应,所以该反应的正反应为放热反应△H<0.②若催化剂的表面积S1>S2。在其它条件不变时,催化剂的表面积越大,反应速率越快,达到平衡所需要的时间就越短。在T1、S2条件下达到平衡过程中的变化曲线为 。
。
练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目

 CH3OH(g) ΔH1 ②CO2(g)+3H2(g)
CH3OH(g) ΔH1 ②CO2(g)+3H2(g)
 2NH3(g)△H=-93.0kJ?mol-1,在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:
2NH3(g)△H=-93.0kJ?mol-1,在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应: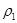
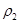
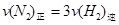 d.混合气体的密度保持不变
d.混合气体的密度保持不变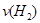 =
= 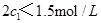 b.氮气的转化率:
b.氮气的转化率: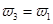 c.
c. 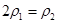 d.
d.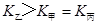
 的电解池,李勇能通过的氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,在电解法合成氨的过程中,应将N2不断地通入 极,该电极反应式为 。
的电解池,李勇能通过的氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,在电解法合成氨的过程中,应将N2不断地通入 极,该电极反应式为 。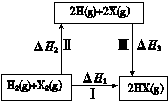


 H+(aq) +CH3COO-(aq) △H2="+1.3" kJ/mol
H+(aq) +CH3COO-(aq) △H2="+1.3" kJ/mol O2(g)=H2O(g)
O2(g)=H2O(g)  kJ·mol-1,② C(s)+
kJ·mol-1,② C(s)+ kJ·mol-1。由此可知焦炭与水蒸气反应的热化学方程式为:C(s)+H2O(g)=CO(g)+H2(g)
kJ·mol-1。由此可知焦炭与水蒸气反应的热化学方程式为:C(s)+H2O(g)=CO(g)+H2(g)  ,则
,则 (NH4)2CO3 (aq) △H1
(NH4)2CO3 (aq) △H1