题目内容
【题目】(2016·新课标全国卷Ⅰ)元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4(绿色)、Cr2O72(橙红色)、CrO42(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(1)Cr3+与Al3+的化学性质相似。在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是_________。
(2)CrO42和Cr2O72在溶液中可相互转化。室温下,初始浓度为1.0 mol![]() L1的Na2CrO4溶液中c(Cr2O72)随c(H+)的变化如图所示。
L1的Na2CrO4溶液中c(Cr2O72)随c(H+)的变化如图所示。
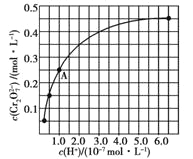
①用离子方程式表示Na2CrO4溶液中的转化反应____________。
②由图可知,溶液酸性增大,CrO42的平衡转化率__________(填“增大”“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为__________。
③升高温度,溶液中CrO42的平衡转化率减小,则该反应的ΔH__0(填“大于”“小于”或“等于”)。
(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl,利用Ag+与CrO42生成砖红色沉淀,指示到达滴定终点。当溶液中Cl恰好沉淀完全(浓度等于1.0×105 mol·L1)时,溶液中c(Ag+)为_______ mol![]() L1,此时溶液中c(CrO42)等于__________ mol
L1,此时溶液中c(CrO42)等于__________ mol![]() L1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×1012和2.0×1010)。
L1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×1012和2.0×1010)。
(4)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72还原成Cr3+,该反应的离子方程式为______________。
【答案】 蓝紫色溶液变浅,同时有灰蓝色沉淀生成,然后沉淀逐渐溶解形成绿色溶液 2CrO42+2H+![]() Cr2O72+H2O 增大 1.0×1014 小于 2.0×105 5×103 Cr2O72+3HSO3 +5H+=2Cr3++3SO42+4H2O
Cr2O72+H2O 增大 1.0×1014 小于 2.0×105 5×103 Cr2O72+3HSO3 +5H+=2Cr3++3SO42+4H2O
【解析】(1)Cr3+与Al3+的化学性质相似,可知Cr(OH)3是两性氢氧化物,能溶解在强碱NaOH溶液中。在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,首先发生反应产生Cr(OH)3灰蓝色固体,当碱过量时,可观察到沉淀消失。故观察到的现象是:蓝紫色溶液变浅,同时有灰蓝色沉淀生成,然后沉淀逐渐溶解直至消失,溶液变为橙红色;(2)①随着H+浓度的增大,CrO42-转化为Cr2O72-的离子反应式为2CrO42-+2H+![]() Cr2O72-+H2O;②溶液酸性增大,平衡2CrO42-+2H+
Cr2O72-+H2O;②溶液酸性增大,平衡2CrO42-+2H+![]() Cr2O72-+H2O正向进行,CrO42的平衡转化率增大;A点Cr2O72-的浓度为0.25mol/L,根据Cr元素守恒可知CrO42-的浓度为0.5mol/L;H+浓度为1×10-7mol/L;此时该转化反应的平衡常数为
Cr2O72-+H2O正向进行,CrO42的平衡转化率增大;A点Cr2O72-的浓度为0.25mol/L,根据Cr元素守恒可知CrO42-的浓度为0.5mol/L;H+浓度为1×10-7mol/L;此时该转化反应的平衡常数为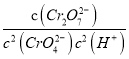 =
=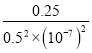 =1014;③升高温度,溶液中CrO42的平衡转化率减小,平衡逆向移动,说明正方向放热,则该反应的ΔH<0;(3)当溶液中Cl-完全沉淀时,即c(Cl-)=1.0×105mol·L1,根据Ksp(AgCl)=2.0×1010,此时c(Ag+)=
=1014;③升高温度,溶液中CrO42的平衡转化率减小,平衡逆向移动,说明正方向放热,则该反应的ΔH<0;(3)当溶液中Cl-完全沉淀时,即c(Cl-)=1.0×105mol·L1,根据Ksp(AgCl)=2.0×1010,此时c(Ag+)=![]() =
=![]() mol·L1=2.0×10-5 mol·L1;此时溶液中c(CrO42)=
mol·L1=2.0×10-5 mol·L1;此时溶液中c(CrO42)=![]() =
=![]() =5×10-3mol·L1;(4)利用NaHSO3的还原性将废液中的Cr2O72还原成Cr3+,发生反应的离子方程式为:Cr2O72-+3HSO3- +5H+=2Cr3++3SO42-+4H2O。
=5×10-3mol·L1;(4)利用NaHSO3的还原性将废液中的Cr2O72还原成Cr3+,发生反应的离子方程式为:Cr2O72-+3HSO3- +5H+=2Cr3++3SO42-+4H2O。

 阅读快车系列答案
阅读快车系列答案【题目】分类、类比是学习化学常用的方法。
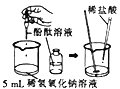
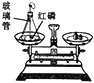
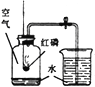
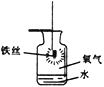
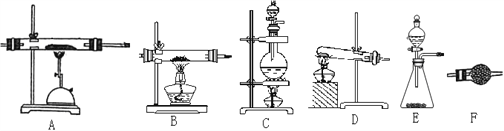
(1)初中化学有许多实验,若按照实验主要目的可将实验分为:探究化学反应前后物质的质量关系、探究物质的性质、探究物质的含量等。据此应将下列实验中的D与________(填“A”或“B”或“C”)归为一类,依据是_______________________________________。
|
|
|
|
A | B | C | D |
(2)实验室现有氯酸钾、稀盐酸、二氧化锰、大理石、火柴、药匙、镊子及以下仪器:
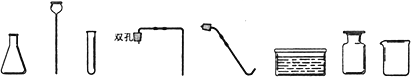
①若补充仪器____________和___________(填名称),并利用上述部分仪器和药品可制取一种气体,则发生反应的化学方程式为____________________________________。
②制取该气体时,需先检查装置的气密性:连接好仪器。将导管一端浸入水中,用手紧握容器外壁,使容器内温度_________,压强变_____,观察到水中导管口有___________时,说明装置不漏气。
(3)许多物质的命名与元素的化合价高低有关,如锰酸钾、高锰酸钾,其中锰元素的化合价分别为+6、+7。氯元素常见的化合价有+7、+5、+1、-1等,由此推测钠元素、氯元素和+7价氯元素三种元素组成的化合物的名称为_____________,化学式为_____________。
【题目】煤燃烧排放的烟气含有SO2和NO,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1在鼓泡反应器中通入含有含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×103mol·L1。反应一段时间后溶液中离子浓度的分析结果如下表;
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/(mol·L1) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式__________________________。增加压强,NO的转化率______(填“提高”“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐______(填“提高”“不变”或“降低”)。
③由实验结果可知,脱硫反应速率______脱硝反应速率(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___________。
(2在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压px如图所示。
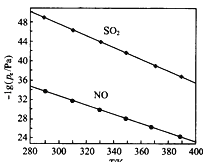
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均______________(填“增大”“不变”或“减小”)。
②反应ClO2+2SO32===2SO42+Cl的平衡常数K表达式为___________。
(3)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。
①从化学平衡原理分析,Ca(ClO)2相比NaClO具有的有点是_______。
②已知下列反应:
SO2(g)+2OH(aq)==SO32(aq)+H2O(l)ΔH1
ClO(aq)+SO32(aq)===SO42(aq)+Cl(aq)ΔH2
CaSO4(s)==Ca2+(aq)+SO42(aq)ΔH3
则反应SO2(g)+Ca2+(aq)+ ClO(aq)+2OH(aq)===CaSO4(s)+H2O(l)+Cl(aq)的ΔH=______。