题目内容
(8分)
(1)已知1.505×1023个X气体分子的质量为8 g ,则该X气体的物质的量为 ,其摩尔质量为 ;
(2)n g O2中有m个O原子,则阿伏加德罗常数NA的数值可表示为
【答案】
(8分) (1)0.25mol; 32g/mol ;(2) 16m/n
【解析】考查物质的量的有关计算。
(1)根据 可知,1.505×1023个X气体分子的物质的量是1.505×1023÷6.02×1023/mol=0.25mol。又因为n=m/M,所以该气体的摩尔质量是8g÷0.25mol=32g/mol。
可知,1.505×1023个X气体分子的物质的量是1.505×1023÷6.02×1023/mol=0.25mol。又因为n=m/M,所以该气体的摩尔质量是8g÷0.25mol=32g/mol。
(2)ng氧气的物质的量是n/32mol,又因为氧气是由2个氧原子构成的,所以根据 可知,阿伏加德罗常数NA的数值可表示为
可知,阿伏加德罗常数NA的数值可表示为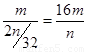 。
。

练习册系列答案
相关题目
(1)已知Na2S2O3+H2SO4═NaSO4+S↓+SO2+H2O.甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如表(所取溶液体积均为10mL):
其他条件不变时:探究温度对化学反应速率的影响,应选择实验 (填实验编号);
若同时选择实验①、实验②、实验③,测定混合液变浑浊的时问,可探究 对化学反应速率的影响.
(2)某同学设计如图实验流程探究Na2S2O3的化学性质.
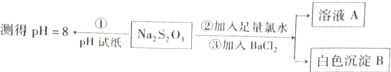
用离子议程式表示Na2S2O3溶液具有碱性的原因 ,实验操作①中测试时pH试纸的颜色应该接近 .
A.红色 B.深蓝色 C.黄色 D.绿色
上述流程中实验②、③的目的是为了探究Na2S2O3某种化学性质,你认为是探究了Na2S2O3的 性.
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol?L-1 | c(H2SO4)/mol?L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
若同时选择实验①、实验②、实验③,测定混合液变浑浊的时问,可探究
(2)某同学设计如图实验流程探究Na2S2O3的化学性质.
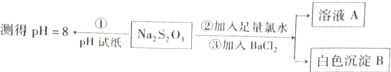
用离子议程式表示Na2S2O3溶液具有碱性的原因
A.红色 B.深蓝色 C.黄色 D.绿色
上述流程中实验②、③的目的是为了探究Na2S2O3某种化学性质,你认为是探究了Na2S2O3的

 钢铁工业在我国国民经济中处于十分重要的位置,工业上采用高炉冶炼,常用赤铁矿、焦炭、空气和熔剂(石灰石)作原料.已知赤铁矿被还原剂还原时是逐级进行的,还原时温度及CO、CO2平衡混合气体中CO的体积分数的关系如图:
钢铁工业在我国国民经济中处于十分重要的位置,工业上采用高炉冶炼,常用赤铁矿、焦炭、空气和熔剂(石灰石)作原料.已知赤铁矿被还原剂还原时是逐级进行的,还原时温度及CO、CO2平衡混合气体中CO的体积分数的关系如图: