题目内容
(1)已知Na2S2O3+H2SO4═NaSO4+S↓+SO2+H2O.甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如表(所取溶液体积均为10mL):| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol?L-1 | c(H2SO4)/mol?L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
若同时选择实验①、实验②、实验③,测定混合液变浑浊的时问,可探究
(2)某同学设计如图实验流程探究Na2S2O3的化学性质.
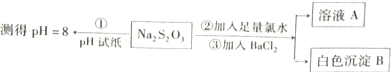
用离子议程式表示Na2S2O3溶液具有碱性的原因
A.红色 B.深蓝色 C.黄色 D.绿色
上述流程中实验②、③的目的是为了探究Na2S2O3某种化学性质,你认为是探究了Na2S2O3的
分析:(1)探究温度对速率的影响时,其他条件要保持不变,使温度成为唯一变量,实验①、实验②和实验③的温度相同,浓度不同,反应物的浓度为变量;
(2)Na2S2O3属于强碱弱酸盐,水解显碱性,PH=8在标准比色卡对应的颜色为绿色;氯水具有强氧化性的溶液,白色沉淀B为硫酸钡.
(2)Na2S2O3属于强碱弱酸盐,水解显碱性,PH=8在标准比色卡对应的颜色为绿色;氯水具有强氧化性的溶液,白色沉淀B为硫酸钡.
解答:解:(1)其他条件不变探究温度对化学反应速率的影响时,要让浓度保持一致,温度成为唯一变量,①⑤和②④这两组浓度一致,因此可选①⑤或②④,实验①、实验②和实验③的温度相同,浓度不同,因此探究的是浓度对化学反应速率的影响,
故答案为:①⑤或②④;比较改变不同反应物的浓度对反应速率的影响;
(2)Na2S2O3属于强碱弱酸盐,在水溶液中可以发生水解,水解的离子方程式为:S2O32-+H2O?HS2O3-+OH-;PH=8对应标准比色卡对应的颜色为绿色;白色沉淀B为硫酸钡,加入氯水的目的是把S2O32-氧化为硫酸根离子,表现了Na2S2O3的还原性,
故答案为:S2O32-+H2O?HS2O3-+OH-;D;还原.
故答案为:①⑤或②④;比较改变不同反应物的浓度对反应速率的影响;
(2)Na2S2O3属于强碱弱酸盐,在水溶液中可以发生水解,水解的离子方程式为:S2O32-+H2O?HS2O3-+OH-;PH=8对应标准比色卡对应的颜色为绿色;白色沉淀B为硫酸钡,加入氯水的目的是把S2O32-氧化为硫酸根离子,表现了Na2S2O3的还原性,
故答案为:S2O32-+H2O?HS2O3-+OH-;D;还原.
点评:本题考查外界条件对化学反应速率的影响,探究单一条件对速率的影响时,要让此条件成为唯一变量,盐类水解的离子方程式书写要注意可逆号,整体难度适中.

练习册系列答案
相关题目