题目内容
下列说法正确的是( )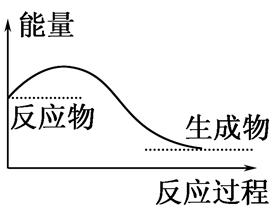
| A.任何化学反应都伴随着能量的变化 |
| B.H2O(g)―→H2O(l)的过程放出大量的热,所以该过程是化学变化 |
| C.化学反应中能量的变化都表现为热量的变化 |
| D.如图所示的是吸收能量的过程 |
A
解析

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
下列反应既是氧化还原反应,又是吸热反应的是( )。
| A.锌粒与稀硫酸的反应 |
| B.灼热的木炭与CO2的反应 |
| C.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应 |
| D.甲烷在空气中燃烧的反应 |
节能减排对发展经济、保护环境有重要意义。下列措施不能减少二氧化碳排放的是( )。
| A.利用太阳能制氢 |
| B.关停小火电企业 |
| C.举行“地球一小时”熄灯活动 |
| D.推广使用煤液化技术 |
下列说法中正确的是( )
| A.物质发生化学反应时都伴随着能量变化,伴随能量变化的物质变化一定是化学变化 |
| B.需要加热的化学反应一定是吸热反应,不需要加热就能进行的反应一定是放热反应 |
| C.吸热反应就是反应物的总能量比生成物的总能量高;也可以理解为化学键断裂时吸收的能量比化学键形成时放出的能量多 |
| D.因为3O2=2O3是吸热反应,所以臭氧比氧气的化学性质更活泼 |
下列说法正确的是 ( )。
| A.任何化学反应都伴随着能量的变化 |
| B.H2O(g)―→H2O(l)该过程放出大量的热,所以该过程是化学变化 |
| C.化学反应中能量的变化都表现为热量的变化 |
| D.对于如图所示的过程,是吸收能量的过程 |

下列分析正确的是( )
| A.将氯气通入H2O2和NaOH的混合溶液中,发出红光,说明反应物的总能量低于生成物的总能量,放出热量 |
| B.1mol H2在氯气中完全燃烧,放出180kJ热量,则键能(E)的关系为E(H—H)=180kJ+2E(H—Cl)-E(Cl—Cl) |
| C.干燥的碘粉与铝粉混合无明显现象,滴上一滴水会冉冉升起紫色的碘蒸气,最后得到白色AlI3。说明碘和铝发生的反应是放热反应 |
| D.精确实验测得H2O在常温下也能微弱电离:H2O??H++OH-,该过程是放热过程 |
下列有关热化学方程式或反应热的说法正确的是( )
A.已知:H2(g)+ O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1,则H2的燃烧热为-241.8 kJ·mol-1 O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1,则H2的燃烧热为-241.8 kJ·mol-1 |
| B.已知:S(g)+O2(g)=SO2(g) ΔH1=-Q1;S(s)+O2(g)=SO2(g) ΔH2=-Q2(Q1、Q2均正值),则Q1<Q2 |
C.已知: H2SO4(浓)+NaOH(aq)= H2SO4(浓)+NaOH(aq)= Na2SO4(aq)+H2O(l) ΔH1;CH3COOH(aq)+NH3·H2O(aq)=CH3COONH4(aq)+H2O(l) ΔH2,则有|ΔH1|<|ΔH2| Na2SO4(aq)+H2O(l) ΔH1;CH3COOH(aq)+NH3·H2O(aq)=CH3COONH4(aq)+H2O(l) ΔH2,则有|ΔH1|<|ΔH2| |
D.已知:Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g) ΔH=+489.0 kJ·mol-1;CO(g)+ O2(g)=CO2(g)ΔH=-283.0 kJ·mol-1;C(石墨,s)+O2(g)=CO2(g)ΔH=-393.5 kJ·mol-1,则4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1641 kJ·mol-1 O2(g)=CO2(g)ΔH=-283.0 kJ·mol-1;C(石墨,s)+O2(g)=CO2(g)ΔH=-393.5 kJ·mol-1,则4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1641 kJ·mol-1 |
下列表述中正确的是( )
A.已知2H2(g)+O2(g) 2H2O(g) ΔH="-483.6" kJ/mol,则氢气的燃烧热为241.8 kJ 2H2O(g) ΔH="-483.6" kJ/mol,则氢气的燃烧热为241.8 kJ |
B.由C(石墨,s) C(金刚石,s) ΔH="+11.9" kJ·mol-1可知,金刚石比石墨稳定 C(金刚石,s) ΔH="+11.9" kJ·mol-1可知,金刚石比石墨稳定 |
C.同温同压下,H2(g)+Cl2(g) 2HCl(g)在光照和点燃条件的ΔH不同 2HCl(g)在光照和点燃条件的ΔH不同 |
| D.任何一个化学变化都伴随着能量的变化 |
已知:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol;②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol。下列结论正确的是( )
| A.碳的燃烧热大于110.5 kJ/mol |
| B.①的反应热为221 kJ/mol |
| C.浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |