��Ŀ����
����Ŀ��ij��ѧ��ȤС����ȡ����غ���ˮ�������й�̽��ʵ�顣
ʵ��� ��ȡ����غ���ˮ
������ͼ��ʾ��ʵ��װ�ý���ʵ�顣

��1��ʢ��Ũ�����ʵ������������________________��
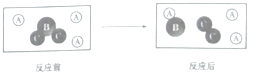
��2��A�з�����Ӧ�Ļ�ѧ��Ӧ����ʽ��_______________��
��3��B����������ص����ӷ�Ӧ����ʽ��_____________��
��4�����Ե�B��Cװ�õ�λ�ã�______ (��ܡ����ܡ�)���B������صIJ��ʣ�ԭ����_____________��
ʵ���� �ⶨԲ����ƿ�з�Ӧ����Һ�������Ũ��
Բ����ƿ���������ķ�Ӧ��������Ũ���½���ֹͣ��Ϊ�ⶨ��Ӧ����Һ�������Ũ�ȣ�̽��С��ͬѧ�������ʵ�鷽����
��������������к͵ζ����ⶨ��
�ҷ�����������Zn��Ӧ���������ɵ�H2�����
�̶���������ʵ�飺
�ٽ��м���ʵ�飺ȷ��ȡ��ȴ��IJ�����Һ��ϡ��һ���ı�������Ϊ������
a����ȡ����20.00mL����0.10 mol��L��1NaOH����Һ�ζ�������ζ��յ�ʱ�����ı���Һ24.00mL����ôεζ����������������Ũ��Ϊ__________��
b���ظ��ζ����κ���ʵ������
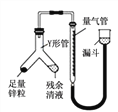
�ڽ����ҷ���ʵ�飺װ������ͼ��ʾ���г���������ȥ����
������ʹY�ι��еIJ�����Һ��п����Ӧ����ȷ�����ǽ�_________
ת�Ƶ�_________�У���������ʵ����ƫ�͡���������Ӧ��ϣ���ȡH2�����������ʱӦע�⣺a.��ȴ�����£�b.________________ c.�����밼Һ����ʹ����С�
���𰸡� ��Һ©�� MnO2+4HCl(Ũ)![]() MnCl2+ Cl2��+2H2O 3Cl2+6OH��
MnCl2+ Cl2��+2H2O 3Cl2+6OH��![]() ClO3��+5Cl��+3H2O �� ˮ��Cl2�е�HCl��ȥ������KOH����ʧ�������KClO3�IJ��� 0.12 mol��L��1 п�� ������Һ ������������©����Һ����ƽ
ClO3��+5Cl��+3H2O �� ˮ��Cl2�е�HCl��ȥ������KOH����ʧ�������KClO3�IJ��� 0.12 mol��L��1 п�� ������Һ ������������©����Һ����ƽ
��������ʵ�����1��ʢ��Ũ�����ʵ�����������Ƿ�Һ©������2��A��Ũ����Ͷ��������ڼ��������·�Ӧ��ȡ������ͬʱ�����Ȼ��̺�ˮ��������Ӧ�Ļ�ѧ��Ӧ����ʽ��MnO2+4HCl(Ũ)![]() MnCl2+ Cl2��+2H2O����3��B����ˮԡ��������Ũ������������Һ��Ӧ��������ء��Ȼ��غ�ˮ�������ӷ�Ӧ����ʽ�ǣ�3Cl2+6OH��
MnCl2+ Cl2��+2H2O����3��B����ˮԡ��������Ũ������������Һ��Ӧ��������ء��Ȼ��غ�ˮ�������ӷ�Ӧ����ʽ�ǣ�3Cl2+6OH��![]() ClO3��+5Cl��+3H2O����4�����Ե�B��Cװ�õ�λ�ã�ˮ��Cl2�е�HCl��ȥ������KOH����ʧ�������B��KClO3�IJ��ʣ�
ClO3��+5Cl��+3H2O����4�����Ե�B��Cװ�õ�λ�ã�ˮ��Cl2�е�HCl��ȥ������KOH����ʧ�������B��KClO3�IJ��ʣ�
ʵ����H����OH����H2O��n(HCl)=n(NaOH)=24��10-3��0.1mol��c��HCl��= ![]() =0.12 mol��L��1����������Ϊʹ��ȫ���μӷ�Ӧ������װ��ͼ��Ӧ��п��ת�Ƶ�������Һ�У�������Ϊ�˷��㻻�㵽��״���£���Ҫ������������©����Һ����ƽ��ʹѹǿ��ȡ�
=0.12 mol��L��1����������Ϊʹ��ȫ���μӷ�Ӧ������װ��ͼ��Ӧ��п��ת�Ƶ�������Һ�У�������Ϊ�˷��㻻�㵽��״���£���Ҫ������������©����Һ����ƽ��ʹѹǿ��ȡ�