题目内容
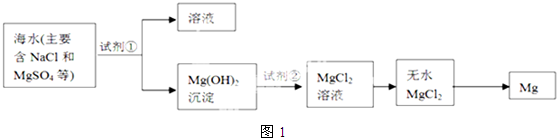
12.实验室用锌跟足量的稀盐酸反应制取氢气,若要制得13.44L(标准状况)氢气,需要多少摩尔锌?需要多少 mL 36.5%的浓盐酸,其密度为1.20g/cm3.?若此浓盐酸稀释至1L后,得到反应所需稀盐酸,则稀盐酸物质的量浓度为多少?(写出计算过程)分析 发生反应:Zn+2HCl=ZnCl2+H2↑,根据n=$\frac{V}{{V}_{m}}$计算氢气物质的量,根据方程式中定比关系计算Zn的物质的量、消耗HCl的物质的量,根据m=nM计算Zn的质量,根据c=$\frac{1000ρω}{M}$计算浓盐酸的物质的量浓度,再根据V=$\frac{n}{c}$计算需要浓盐酸体积,根据稀释定律计算稀释后盐酸的浓度.
解答 解:标况下13.44L氢气的物质的量为$\frac{13.44L}{22.4L/mol}$=0.6mol
Zn+2 HCl=ZnCl2+H2↑
1 2 1
0.6mol 1.2mol 0.6mol
36.5%的浓盐酸,其密度为1.20g/cm3,则其物质的量浓度=$\frac{1000×1.2×36.5%}{36.5}$mol/L=12mol/L,故消耗浓盐酸的体积为$\frac{1.2mol}{12mol/L}$=0.1L,即为100mL;
若此浓盐酸稀释至1L后,则所得稀盐酸的浓度为$\frac{0.1L×12mol/L}{1L}$=1.2mol/L,
答:反应消耗Zn为0.6mol;需要浓盐酸的体积为100mL,稀释后盐酸的浓度为1.2mol/L.
点评 本题考查化学方程式有关计算、物质的量浓度计算,难度不大,注意理解掌握物质的量浓度与质量分数之间的关系.

练习册系列答案
相关题目
2.过氧化氢,熔点-0.41℃.沸点150.2℃.无色透明液体,溶于水、醇、乙醚.具有较强的氧化能力,为强氧化剂.当遇热、光、粗糙表面、重金属、二氧化锰及其他杂质时,则发生剧烈分解,并放出大量的热,与可燃物接触可产生氧化自燃.化学工业上常用作制造过碳酸钠、过氧乙酸等过氧化物的原料;在生活中主要用作食品加工、食品的漂白、防腐和保鲜剂.某班同学在学习完过课本有关过氧化氢性质后,分成甲、乙、丙三组分别开展了相关的探究活动.现请就他们活动中的一些内容回答下列问题.

1.甲组同学以“寻找常温下能加速过氧化氢分解的催化剂,并通过实验比较它们的效果”为课题开展研究,
(1)经过初步研究,他们选定了五种物质进行两两对比实验.下列实验组不可能为相应的猜想提供证据的是A
(2)他们在对比实验过程中的如下操作,你认为不正确的是D
A.在同组实验时,都使用量筒量取相同量的过氧化氢溶液
B.在同组实验时,都使用托盘天平称取相同量的固体样品
C.在同组实验时,控制同组实验的浓度、用量等条件一致
D.在同组实验时,其中一个实验使用酒精灯加热
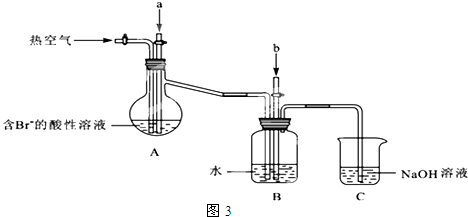
(3)图1是他们设计的四组实验装置.在两两对比实验中,下列观察(或测定)方法最难以比较样品对过氧化氢分解加速效果的是C
A.第一组是同时实验,观察比较反应过程中两个气球体积的变化情况
B.第二组是同时实验,观察比较反应过程中两者产生气泡的快慢
C.第三组是分两次实验,看木条是否能复燃
D.第四组是分两次实验,比较反应过程中收集一定体积氧气所需的时间
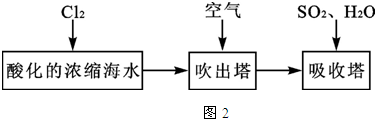
2.乙组用市售过氧化氢溶液配成15%左右过氧化氢溶液,采用下列装置如图2(装置气密性良好)以过氧化氢代替氯酸钾制取氧气.进行实验.在有不少气泡产生数分钟后,用排空气法收集一试管气体,用带火星的木条检验.带火星的木条并不复燃.
a.加热的时间还不够长,试管内氧气的蓄积量不够多(观察与猜想).
b.产生气泡的速度太慢,应提高温度加快产生气泡的速度(观察与假设).
c.过氧化氢溶液浓度过小.
增大过氧化氢溶液的浓度,延长加热时间,在反应速率明显加快的情况下,用带火星木条检验,仍不复燃.
在经过重新讨论后,该小组同学将收集气体的方法改为排水法收集后,并用带火星木条检验,木条复燃.则原先带火星木条并不复燃的原因可能是:a.加热时产生的氧气在温度较高时形成热气流逸散到试管口外的空气中.b.过氧化氢溶液中水的含量超过过氧化氢的含量,加热时除产生氧气而外,还产生大量水蒸汽,致使试管内氧气的含量过少.
3.丙组同学将H2O2溶液滴入含有酚酞的NaOH中,发现红色消失.A同学认为这是由于H2O2是二元弱酸(H2O2?H++HO2-),消耗了OH-,而使红色褪去.B同学认为H2O2具有强氧化性,将酚酞氧化,红色消去.试设计实验论证两位同学的解释中谁正确:a.加热时产生的氧气在温度较高时形成热气流逸散到试管口外的空气中;b.过氧化氢溶液中水的含量超过过氧化氢的含量,加热时除产生氧气而外,还产生大量水蒸汽,致使试管内氧气的含量过少.

1.甲组同学以“寻找常温下能加速过氧化氢分解的催化剂,并通过实验比较它们的效果”为课题开展研究,
(1)经过初步研究,他们选定了五种物质进行两两对比实验.下列实验组不可能为相应的猜想提供证据的是A
| 组 别 | 猜 想 | 实验组 |
| A | 较活泼金属的氧化物催化效果好 | 氧化铁和铁丝 |
| B | 较活泼的金属单质催化效果好 | 铜丝和铁丝 |
| C | 高价的金属氧化物催化效果好 | 氧化亚铁和氧化铁 |
| D | 氧化物比单质催化效果好 | 氧化铜和铜丝 |
A.在同组实验时,都使用量筒量取相同量的过氧化氢溶液
B.在同组实验时,都使用托盘天平称取相同量的固体样品
C.在同组实验时,控制同组实验的浓度、用量等条件一致
D.在同组实验时,其中一个实验使用酒精灯加热
(3)图1是他们设计的四组实验装置.在两两对比实验中,下列观察(或测定)方法最难以比较样品对过氧化氢分解加速效果的是C
A.第一组是同时实验,观察比较反应过程中两个气球体积的变化情况
B.第二组是同时实验,观察比较反应过程中两者产生气泡的快慢
C.第三组是分两次实验,看木条是否能复燃
D.第四组是分两次实验,比较反应过程中收集一定体积氧气所需的时间
2.乙组用市售过氧化氢溶液配成15%左右过氧化氢溶液,采用下列装置如图2(装置气密性良好)以过氧化氢代替氯酸钾制取氧气.进行实验.在有不少气泡产生数分钟后,用排空气法收集一试管气体,用带火星的木条检验.带火星的木条并不复燃.
a.加热的时间还不够长,试管内氧气的蓄积量不够多(观察与猜想).
b.产生气泡的速度太慢,应提高温度加快产生气泡的速度(观察与假设).
c.过氧化氢溶液浓度过小.
增大过氧化氢溶液的浓度,延长加热时间,在反应速率明显加快的情况下,用带火星木条检验,仍不复燃.
在经过重新讨论后,该小组同学将收集气体的方法改为排水法收集后,并用带火星木条检验,木条复燃.则原先带火星木条并不复燃的原因可能是:a.加热时产生的氧气在温度较高时形成热气流逸散到试管口外的空气中.b.过氧化氢溶液中水的含量超过过氧化氢的含量,加热时除产生氧气而外,还产生大量水蒸汽,致使试管内氧气的含量过少.
3.丙组同学将H2O2溶液滴入含有酚酞的NaOH中,发现红色消失.A同学认为这是由于H2O2是二元弱酸(H2O2?H++HO2-),消耗了OH-,而使红色褪去.B同学认为H2O2具有强氧化性,将酚酞氧化,红色消去.试设计实验论证两位同学的解释中谁正确:a.加热时产生的氧气在温度较高时形成热气流逸散到试管口外的空气中;b.过氧化氢溶液中水的含量超过过氧化氢的含量,加热时除产生氧气而外,还产生大量水蒸汽,致使试管内氧气的含量过少.
3.某种飞船以N2H4和N2O4为动力源,发生反应:2N2H4+N2O4═3N2↑+4H2O,反应温度可高达2700℃,若有1mol N2H4被氧化,则下列判断不正确的是( )
| A. | 生成33.6LN2(标准状况下) | B. | 被还原的N原子的物质的量为2mol | ||
| C. | 转移电子的物质的量为4 mol | D. | 还原产物比氧化产物多0.5mol |
7.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 6.0gSiO2晶体中含有0.2NA个Si-O键 | |
| B. | 1L1mol•L-1CH3COOH溶液中,所含CH3COO-、CH3COOH的总数为NA | |
| C. | 1L1mol•L-1饱和FeCl3溶液滴入沸水中完全水解生成Fe(OH)3胶体粒子数为NA个 | |
| D. | 10g46%的乙醇水溶液中所含H原子数为0.6NA |
17.某反应过程中体系的能量变化如图所示,下列说法错误的是( )


| A. | 反应过程可表示为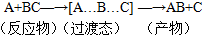 | |
| B. | E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能 | |
| C. | 此图中逆反应的热效应△H=E1-E2,为吸热反应 | |
| D. | 此图中正反应的热效应为△H=E1-E2,且E2>E1,所以正反应为放热反应 |
4.下列各组物质中,两者互为同分异构体的是( )
| A. | 2CaSO4•H2O和CaSO4•2H2O | B. | CH3CH2OH与CH3OCH3 | ||
| C. | CuSO4•3H2O与CuSO4•5H2O | D. | H2O与D2O(重水) |