题目内容
【题目】有X、Y、Z、Q、T五种元素,X原子的M层p轨道有2个未成对电子,Y原子的外围电子构型为3d64s2,Z原子的L电子层的p能级上有一空轨道,Q原子的L电子层的p能级上只有1对成对电子,T原子的M电子层上p轨道半充满。试写出:
(1)X的元素符号____,Y的元素符号___。
(2)Z的电子排布式___,Q的电子排布式___。
(3)Y的单质在Q的单质中燃烧的化学方程式___。
【答案】S Fe 1s22s22p2 1s22s22p4 3Fe+2O2![]() Fe3O4
Fe3O4
【解析】
5种元素X、Y、Z、Q、T,X原子M层上有2个未成对电子且无空轨道,外围电子排布式为3s23p4,则X为S元素;Y原子的外围电子排布为3d64s2,则Y为Fe元素;Z原子的L电子层的p能级上有一个空轨道,外围电子排布式为2s22p2,则Z为C元素;Q原子的L电子层的P能级上只有一对成对电子,外围电子排布式为2s22p4,则Q是O元素;T原子的M电子层上p轨道半充满,外围电子排布式为3s23p3,则T是P元素,据此分析解答。
(1)根据上述分析可知,X是S元素,Y是Fe元素,故答案为:S;Fe;
(2)Z为C元素,核电荷数为6,电子排布式为:1s22s22p2,Q为氧元素,氧原子的核外电子排布式为:1s22s22p4,故答案为:1s22s22p2;1s22s22p4;
(3)Y的单质在Q的单质中燃烧是铁在纯氧中燃烧生成四氧化三铁,反应的化学方程式为:3Fe+2O2![]() Fe3O4,故答案为:3Fe+2O2
Fe3O4,故答案为:3Fe+2O2![]() Fe3O4。
Fe3O4。

 阅读快车系列答案
阅读快车系列答案【题目】氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用。
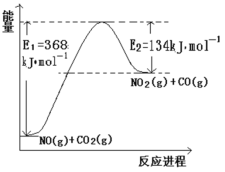
⑴根据下面能量变化示意图,请写出 NO 和 CO2反应的热化学方程式_________。
⑵在固定体积的密闭容器中,进行如下化学反应:2NH3(g)![]() N2(g)+3H2(g) △H>0,其平衡常数 K 与温度 T 的关系如下表:
N2(g)+3H2(g) △H>0,其平衡常数 K 与温度 T 的关系如下表:
T/K | 298 | 398 | 498 |
平衡常数K | 4.1×106 | K1 | K2 |
①试判断 K1_________K2(填写“>”,“<”或“=”);
②该反应的熵变S_________0(填 >、< 或 = )
③下列各项能说明该反应已达到平衡状态的是_________(填字母);
a.容器内N2、H2、NH3的物质的量之比为1∶3∶2 b.2υ(NH3)正 = 3υ(H2)逆
c.容器内混合气体平均相对分子质量保持不变 d.混合气体的密度保持不变
④一定温度下,在 1L 密闭容器中充入 1molN2和 3molH2 并发生反应。若容器容积恒定,10min 达到平衡时,气体的总物质的量为原来的9/10,则N2的转化率![]() (N2)=_________________
(N2)=_________________
⑶对反应 N2O4(g)![]() 2NO2(g) △H > 0 ,在温度分别为T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如右图所示,下列说法正确的是__________。
2NO2(g) △H > 0 ,在温度分别为T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如右图所示,下列说法正确的是__________。
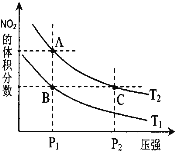
a.A、C 两点的反应速率:A>C
b.A、C 两点的化学平衡常数:A>C
c.A、C 两点 N2O4的转化率:A>C
d.由状态 B 到状态 A,可以用加热的方法