题目内容
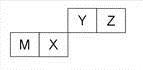
短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y、Z原子序数之和是W的2倍,X、Z在周期表中的相对位置如图所示,X的最低负价绝对值与其原子最外层电子数相等。下列说法不正确的是


| A.原子半径:Y>Z>W |
| B.一定条件下,Y可置换出X |
| C.气态氢化物稳定性:Z>W |
| D.熔点YW2>XW4 |
C
试题分析:短周期元素X的最低负价绝对值与其原子最外层电子数相等,则X为C;Z为S;W是Cl. 因为X、Y、Z原子序数之和是W的2倍,所以Y的原子序数为2×17-6-16=12.所以Y为Mg。A.Mg、S、Cl是同一周期的元素。随着原子序数的增大,原子半径逐渐减小。所以原子半径:Mg>S>Cl。正确。B.在点燃情况下可以发生反应:2Mg+CO2
 2MgO+C.正确。C.非金属性Cl>S.元素的非金属性越强,其对应的气态氢化物稳定性就大。所以氢化物的稳定性:HCl>H2S。错误。D.MgCl2是离子化合物,离子间以离子键结合,断裂要消耗较多的能量,所以熔沸点较高,而CCl4是由分子构成的物质。分子间以分子间作用力结合。分子间作用力比化学键弱得多,断裂较容易。所以熔沸点较低。因此熔点:MgCl2>CCl4。正确。
2MgO+C.正确。C.非金属性Cl>S.元素的非金属性越强,其对应的气态氢化物稳定性就大。所以氢化物的稳定性:HCl>H2S。错误。D.MgCl2是离子化合物,离子间以离子键结合,断裂要消耗较多的能量,所以熔沸点较高,而CCl4是由分子构成的物质。分子间以分子间作用力结合。分子间作用力比化学键弱得多,断裂较容易。所以熔沸点较低。因此熔点:MgCl2>CCl4。正确。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目