题目内容
【题目】下列各组物质:①O2和O3 ②H2、D2、T2 ③12 C和14 C
④CH3CH2CH2CH2CH3和(CH3)2CHCH2CH3 ⑤癸烷和十六烷 ⑥CH3(CH2)5CH3和CH3CH2CH(CH3)C2H5
⑦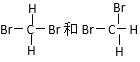
A、互为同位素的是_________;B、互为同分异构体的是________;
C、互为同素异形体的是________;D、同一种物质的是_________。
【答案】 ③ ④⑥ ① ②⑦
【解析】①O2和O3 是同种元素所形成的性质不同的单质,互为同素异形体;②H2、D2、T2 都是氢元素组成的氢气分子,属于同种物质;③12C和14C 中子数不同,是碳元素的不同原子,互为同位素;④CH3CH2CH2CH2CH3和(CH3)2CHCH2CH3分子式相同,结构不同,为碳链异构,互为同分异构体;⑤癸烷和十六烷 结构相似,都属于烷烃,分子组成上相差6个CH2原子团;⑥CH3(CH2)5CH3和CH3CH2CH2CH(CH3)C2H5 分子式相同,结构不同,为碳链异构,互为同分异构体;⑦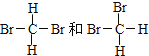 都是甲烷的二溴代物,属于同种物质;A、互为同位素故选③;B、互为同分异构体故选④⑥;C、互为同素异形体故选①;D、同一种物质故选②⑦;故答案为:③;④⑥;①;②⑦。
都是甲烷的二溴代物,属于同种物质;A、互为同位素故选③;B、互为同分异构体故选④⑥;C、互为同素异形体故选①;D、同一种物质故选②⑦;故答案为:③;④⑥;①;②⑦。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
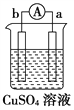
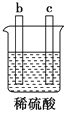
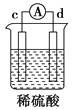
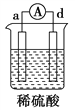
【题目】有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验 装置 |
装置一 |
装置二 |
装置三 |
装置四 |
部分实验现象 | a极质量减小,b极质量增大 | b极有气体产生,c极无变化 | d极溶解,c极有气体产生 | 电流从a极 流向d极 |
由此可判断这四种金属活动性顺序是( )
A. a>b>c>d B. b>c>d>a C. a>b>d>c D. d>a>b>c