题目内容
【题目】无水氯化铝是一种重要的化工原料,工业上利用明矾石制备无水氯化铝的流程如图,请回答下列问题: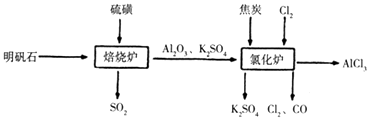
(1)实验室中,可制得Cl2的组合是(填代号).
①MnO2和浓盐酸混合共热 ②MnO2、NaCl和浓硫酸混合共热
③NaClO和盐酸混合共热 ④漂白粉和硫酸混合共热
(2)吸收焙烧炉中产生的尾气,下列装置合理的是(填代号).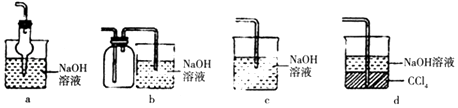
(3)写出氧化炉中反应的化学方程式
(4)生产氯化铝的过程中焙烧炉和氯化炉中产生的SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少污染.试设计简单实验检验二者是否恰好完全反应,简要描述实验步骤、现象和结论(仪器自选).
可供选择试剂如下:
①滴加酚酞的氢氧化钠溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④品红溶液
(5)某同学设计用如图装置验证二氧化硫的某些化学性质.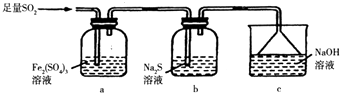
①能说明二氧化硫具有氧化性的实验现象为 .
②写出a瓶中发生反应的离子方程式 .
③充分反应后,取a瓶中的溶液分成三份,分别进行如下实验.
实验I:向第一份溶液中加入足量的NaOH溶液,生成白色沉淀,迅速变为灰绿色,最终变为红褐色.
实验II:向第二份溶液中加入少量KMnO4溶液,紫色褪去.
实验III:向第三份溶液中加入BaCl2溶液,生成白色沉淀.
上述实验中能充分证明二氧化硫具有还原性的是:(填实验代号).
【答案】
(1)①②③④
(2)ad
(3)3C+Al2O3+3Cl2 ![]() 3CO+2AlCl3
3CO+2AlCl3
(4)取二者溶于水后的溶液少许置于试管中,向其中加入品红溶液,若品红不褪色,说明二者恰好完全反应,否则,两者未完全反应
(5)b中出现淡黄色沉淀;2Fe3++SO2+2H2O=2Fe2++SO42﹣+4H+;Ⅰ和Ⅱ
【解析】解:(1)①MnO2和浓盐酸混合共热生成氯化锰、氯气和水,故正确;
②NaCl和浓硫酸混合共热能生成浓盐酸再与MnO2混合共热生成氯化锰、氯气和水,故正确;
③NaClO和盐酸混合共热,其中次氯酸根、氢离子、氯离子混合反应生成氯气和水,故正确;
④漂白粉和硫酸混合共热,其中次氯酸根、氢离子、氯离子混合反应生成氯气和水,故正确;
故选:①②③④;(2)a.干燥管球形处容积较大,溶液倒吸后会于烧杯内的液体分离,由重力作用又回到烧杯内,可以防止倒吸,故a正确;
b.广口瓶中进气管长,出气管短,不能防止倒吸,应进气管短,故b错误;
c.导管直接伸入液面内,会发生倒吸危险,故c错误;
d.二氧化硫经过四氯化碳后,被氢氧化钠溶液吸收,可以防止倒吸,故d正确,
故选:ad;(3)由流程图可知,氯化炉中氧化铝、碳、氯气反应生成氯化铝、CO,反应方程式为:3C+Al2O3+3Cl2 ![]() 3CO+2AlCl3 , 所以答案是:3C+Al2O3+3Cl2
3CO+2AlCl3 , 所以答案是:3C+Al2O3+3Cl2 ![]() 3CO+2AlCl3;(4)取二者溶于水后的溶液少许置于试管中,向其中加入品红溶液,若品红不褪色,说明二者恰好完全反应,否则,两者未完全反应,
3CO+2AlCl3;(4)取二者溶于水后的溶液少许置于试管中,向其中加入品红溶液,若品红不褪色,说明二者恰好完全反应,否则,两者未完全反应,
所以答案是:取二者溶于水后的溶液少许置于试管中,向其中加入品红溶液,若品红不褪色,说明二者恰好完全反应,否则,两者未完全反应;(5)①硫化钠溶液里通SO2发生反应的离子方程式为SO2+2S2﹣+2H2O=3S↓+4OH﹣ , 此反应体现了SO2的氧化性,看到的现象是b中出现淡黄色沉淀,所以答案是:b中出现淡黄色沉淀;
②二氧化硫能被硫酸铁溶液氧化,生成硫酸根离子和亚铁离子,反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42﹣+4H+ ,
所以答案是:2Fe3++SO2+2H2O=2Fe2++SO42﹣+4H+;
③实验Ⅰ中有氢氧化亚铁沉淀生成,实验Ⅱ中有亚铁离子生成,都说明二氧化硫将铁离子还成亚铁离子,说明二氧化硫具有还原性,所以实验Ⅰ和Ⅱ都说明二氧化硫具有还原性,所以答案是:Ⅰ和Ⅱ.