��Ŀ����
����Ŀ��I����ѧ��Ӧԭ����
���º����£���2mol����A��2mol����Bͨ�����Ϊ2L���ܱ������У��������·�Ӧ��2A(g)+B(g)![]() xC(g)+2D(s)��2min��Ӧ�ﵽƽ��״̬����ʱʣ��1.2mol B�������C��Ũ��Ϊ1.2mol/L��
xC(g)+2D(s)��2min��Ӧ�ﵽƽ��״̬����ʱʣ��1.2mol B�������C��Ũ��Ϊ1.2mol/L��
��1���ӿ�ʼ��Ӧ��ƽ��״̬������C��ƽ����Ӧ����Ϊ__________��
��2��x=_________���÷�Ӧ�Ļ�ѧƽ�����ʽΪ________________��
��3��A��ת������B��ת����֮��Ϊ________��
��4�����и������Ϊ�÷�Ӧ�ﵽƽ��״̬�ı�־��_______ (����ĸ)��
A.ѹǿ���ٱ仯 B.�����ܶȲ��ٱ仯
C.����ƽ����Է����������ٱ仯 D. A������������B����������֮��Ϊ2:1
II (��ѧ������)
����Ӫ��ƽ�⡢��ѧʹ��ʳƷ���Ӽ�������ʹ��ҩ������ڽ������������������������
����ͼΪijƷ�Ƽ�����ǩ��һ���֣�������ˮ�����ɰ������������________��������ɫ������_____�����ڷ���������____________��

����һ֧ʢ��2mL2%������Һ���Թ��е���2�ε�ˮ����Һ����ɫ���ٵ���ά����C��ˮ��Һ����Һ��ɫ�仯��__________����ʵ��˵��ά����C����___________�ԣ�ѡ����ᡱ������������ԭ������
���𰸡� 0.6mol/(L��min) 3 K=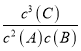 2:1 BC ����� ���� ɽ���� ����ɫ����ɫ ��ԭ
2:1 BC ����� ���� ɽ���� ����ɫ����ɫ ��ԭ
��������I����1���ӿ�ʼ��Ӧ��ƽ��״̬������C��ƽ����Ӧ����Ϊ1.2mol/L��2min��0.6mol/(L��min)����2������B�����ʵ�����2mol��1.2mol��0.8mol������C��2.4mol�����ݱ仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪x=3��D�ǹ��壬���Ը÷�Ӧ�Ļ�ѧƽ�����ʽΪK= ����3������A��1.6mol����A��ת������B��ת����֮��Ϊ
����3������A��1.6mol����A��ת������B��ת����֮��Ϊ![]() ����4��A.��Ӧǰ��������䣬��ѹǿ���ٱ仯����˵����Ӧ�ﵽƽ��״̬��A����B. �ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������ݻ�ʼ���Dz���ģ�������������DZ仯�ģ����������ܶȲ��ٱ仯��˵����Ӧ�ﵽƽ��״̬��B��ȷ��C. �������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ�����ʵ������䣬�������DZ仯�ģ���������ƽ����Է����������ٱ仯��˵����Ӧ�ﵽƽ��״̬��C��ȷ��D. ���ݷ���ʽ��֪A������������B����������֮��ʼ��Ϊ2:1�����Բ��ܾݴ�˵����Ӧ�ﵽƽ��״̬��D����ѡBC��
����4��A.��Ӧǰ��������䣬��ѹǿ���ٱ仯����˵����Ӧ�ﵽƽ��״̬��A����B. �ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������ݻ�ʼ���Dz���ģ�������������DZ仯�ģ����������ܶȲ��ٱ仯��˵����Ӧ�ﵽƽ��״̬��B��ȷ��C. �������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ�����ʵ������䣬�������DZ仯�ģ���������ƽ����Է����������ٱ仯��˵����Ӧ�ﵽƽ��״̬��C��ȷ��D. ���ݷ���ʽ��֪A������������B����������֮��ʼ��Ϊ2:1�����Բ��ܾݴ�˵����Ӧ�ﵽƽ��״̬��D����ѡBC��
II���ٵ�����ˮ�����ɰ����������������ˮ�����ɰ�����������Ǽ���ۣ�������ɫ�����ǽ��ƣ����ڷ���������ɽ���ᡣ��ά����C���л�ԭ�ԣ��ܱ���ˮ���������ʵⱻ��ԭ��������Һ��ɫ�仯������ɫ����ɫ��

 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�����Ŀ����3�ֲ�ͬ�����£��ֱ����ݻ�Ϊ2L�ĺ����ܱ������г���2molA��1molB��������Ӧ:2A(g)+B(g)![]() 2D(g)��H=QkJ/mol��������������ݼ��±�:
2D(g)��H=QkJ/mol��������������ݼ��±�:
ʵ���� | ʵ��I | ʵ��II | ʵ��III |
��Ӧ�¶�/�� | 700 | 700 | 750 |
��ƽ��ʱ��/min | 40 | 50 | 30 |
n(D)ƽ��/mol | 1.5 | 1.5 | 1 |
��ѧƽ�ⳣ�� | K1 | K2 | K3 |
����˵����ȷ����
A. �����¶��ܼӿ췴Ӧ���ʵ�ԭ���ǽ����˷�Ӧ�Ļ�ܣ�ʹ����Ӱٷ������
B. ʵ��III��ƽ����������������䣬����������ͨ��1molA��1molD��ƽ�ⲻ�ƶ�
C. ʵ��III��ƽ��������ڵ�ѹǿ��ʵ��1��9/10��
D. K3>K2>K1