题目内容
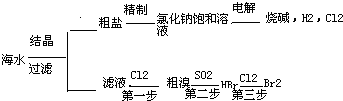
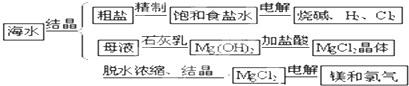
海水中有取之不尽的化学资源,从海水中可提取多种化工原料.下图是某工厂对海水资源的综合利用的示意图.
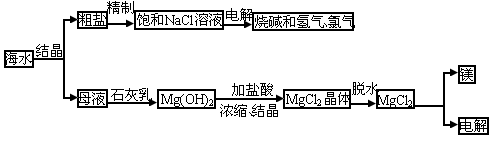
试回答下列问题:
(1)粗盐中含有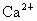 、
、 、
、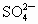 等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中依次加入过量的
等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中依次加入过量的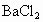 溶液、过量的NaOH溶液和过量的
溶液、过量的NaOH溶液和过量的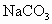 溶液,最后加入盐酸至溶液呈中性.
溶液,最后加入盐酸至溶液呈中性.
请写出加入盐酸后可能发生的化学反应的离子方程式:______________.
(2)海水提取食盐后的母液中有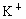 、
、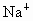 、
、 等阳离子.从离子反应的角度思考,在母液里加入石灰乳起什么作用?
等阳离子.从离子反应的角度思考,在母液里加入石灰乳起什么作用?
(3)海水里的镁元素处于游离态还是化合态?从海水中提取氯化镁的反应是不是氧化还原反应?用电解法冶炼金属镁的反应是不是氧化还原反应?为什么?
(4)电解无水氯化镁所得的镁蒸气冷却后即为固体镁。请思考镁蒸气可以在下列哪种气体氛围中冷却( )
A.H2 B.CO2 C.空气 D.O2
答案:略
解析:
解析:
|
(1) (2) 石灰乳作沉淀剂,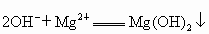 ,使 ,使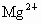 以沉淀的形式分离出来,便于后续操作. 以沉淀的形式分离出来,便于后续操作.
(3) 化合态.从海水中提取氯化镁的过程并不涉及元素化合价的变化,因此是非氧化还原反应.电解法冶炼金属镁时,镁的化合价由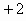 价降低到0价,氯的化合价由 价降低到0价,氯的化合价由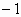 价升高到0价,因此该反应是氧化还原反应. 价升高到0价,因此该反应是氧化还原反应.
(4)A 以海水资源的综合利用为载体,分别考查了离子反应方程式的书写、离子反应、氧化还原反应知识、金属镁的有关性质. (1)加入氯化钡时,主要是除去粗盐溶液中的 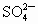 , ,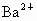 与其中的生成 与其中的生成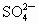 沉淀: 沉淀: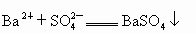 ;过量的NaOH溶液则是为了除去 ;过量的NaOH溶液则是为了除去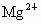 : :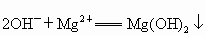 ;过量的 ;过量的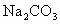 溶液中的 溶液中的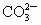 则和 则和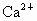 、之前加入的过量的 、之前加入的过量的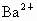 发生离子反应: 发生离子反应: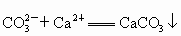 , ,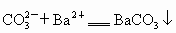 ,此时溶液中的溶质主要为NaCl和 ,此时溶液中的溶质主要为NaCl和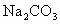 ;最后加入盐酸是为了调节溶液的pH,除去过量的 ;最后加入盐酸是为了调节溶液的pH,除去过量的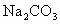 . .
(2)加入石灰乳的目的是为了使 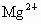 以沉淀的形式分离出来,便于后续操作. 以沉淀的形式分离出来,便于后续操作.
(3)海水中的镁是以盐的形式存在,其中镁元素处于化合态.从海水中提取氯化镁的过程并不涉及元素化合价的变化,因此是非氧化还原反应.电解法冶炼金属镁时,镁的化合价由 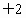 价降低到0价,氯的化合价由 价降低到0价,氯的化合价由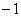 价升高到0价,因此该反应是氧化还原反应. 价升高到0价,因此该反应是氧化还原反应.
(4)预习下一作业的内容可知金属镁的化学性质. |

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目