题目内容
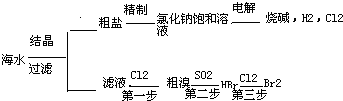
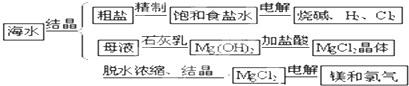
海水中有取之不尽的化学资源,从海水中可提取多种化工原料,下图是某工厂对海水资源的综合利用的示意图:
回答下列问题:
(1)操作A的实验名称为:
(2)镁是活泼的金属,能在二氧化碳中燃烧,反应方程式为:

回答下列问题:
(1)操作A的实验名称为:
过滤
过滤
,B的化学式为NaOH
NaOH
(2)镁是活泼的金属,能在二氧化碳中燃烧,反应方程式为:
2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
.
| ||
分析:(1)根据生石灰和水反应能生成氢氧化钙,氢氧化钙和氯化镁反应能生成氢氧化镁沉淀和氯化钙,过滤即可得氢氧化镁沉淀;电解饱和食盐水得到氢氧化钠、氢气、氯气;
(2)根据镁和二氧化碳的反应生成碳和氧化镁;
(2)根据镁和二氧化碳的反应生成碳和氧化镁;
解答:解:(1)生石灰和水反应能生成氢氧化钙,氢氧化钙和氯化镁反应能生成氢氧化镁沉淀和氯化钙,过滤即可得氢氧化镁沉淀,所以操作A的实验名称为过滤;电解饱和食盐水得到氢氧化钠、氢气、氯气,所以B的化学式为NaOH,故答案为:过滤;NaOH;
(2)镁和二氧化碳的反应生成碳和氧化镁,方程式为:2Mg+CO2
2MgO+C;
故答案为:2Mg+CO2
2MgO+C;
(2)镁和二氧化碳的反应生成碳和氧化镁,方程式为:2Mg+CO2
| ||
故答案为:2Mg+CO2
| ||
点评:本题考查工业制镁、氯碱工业以及镁的化学性质,难度不大,要求同学们对课本知识能够牢固的掌握.

练习册系列答案
相关题目