题目内容
【题目】(1)请正确表示下列化学用语:乙炔(结构式)__________;甲烷(空间构型)_________;羟基(电子式)_________;C22-(电子式)_________ ;异戊二烯(结构简式)______________。
(2)高分子化合物![]() 是由三种单体通过加聚反应而制得的。这三种单体的结构简式是____________、____________、____________;
是由三种单体通过加聚反应而制得的。这三种单体的结构简式是____________、____________、____________;
(3)书写化学方程式并注明反应类型(有机物写结构简式):
①CH3-CH2-Br与氢氧化钠溶液在加热条件下的反应方程式:_______________________(____________);
②甲苯制备TNT:__________________________(_____________)。
【答案】H—C≡C—H 正四面体形 ![]()
![]()
![]()
![]() CH≡CH CH2=CH-CH3 CH3-CH2-Br+NaOH
CH≡CH CH2=CH-CH3 CH3-CH2-Br+NaOH![]() CH3-CH2-OH +NaBr 水解反应或者取代反应
CH3-CH2-OH +NaBr 水解反应或者取代反应 ![]() +3HNO3(浓)
+3HNO3(浓) ![]()
 +3H2O 硝化反应或取代反应
+3H2O 硝化反应或取代反应
【解析】
(1)乙炔分子中含有碳碳三键;甲烷是正四面体结构;氢一氧原子形成一个共价键;C22-中两个C原子共用3对电子,每个C再获得1个电子,从而使每个原子达到8个电子的稳定结构;异戊二烯是2-甲基-1,3-丁二烯的结构;
(2)聚合物链节中,从碳碳双键两端往外的第2个C原子处断裂化学键,单键变双键,双键变单键,若无双键,就2个C原子处断裂碳碳键,判断聚合物的单体;
(3)①CH3-CH2-Br与氢氧化钠溶液在加热发生取代反应产生乙醇;
②甲苯与浓硝酸在加热时发生取代反应制备三硝基甲苯,即产生TNT。
(1)乙炔分子中两个C原子形成三对共用电子对,每个C原子再与H原子形成一对共用电子对,所以乙炔的结构式为H—C≡C—H;甲烷分子中C原子与4个H原子形成4对共用电子对,空间构型是正四面体形;羟基是O原子与H原子形成了1对共用电子对,所以羟基的电子式为![]() ;C22-中2个C原子形成3对共用电子对,每个C原子再获得1个电子,所以C22-的电子式为
;C22-中2个C原子形成3对共用电子对,每个C原子再获得1个电子,所以C22-的电子式为![]() ;异戊二烯是2-甲基-1,3-丁二烯,因此其结构简式为
;异戊二烯是2-甲基-1,3-丁二烯,因此其结构简式为![]() 。
。
(2)高分子化合物![]() 是由三种单体通过加聚反应而制得的。这三种单体的结构简式是
是由三种单体通过加聚反应而制得的。这三种单体的结构简式是![]() 、CH≡CH、CH2=CH-CH3;
、CH≡CH、CH2=CH-CH3;
(3)①CH3-CH2-Br与氢氧化钠溶液在加热条件下发生取代反应产生乙醇和NaBr,反应方程式:CH3-CH2-Br+NaOH![]() CH3-CH2-OH +NaBr;
CH3-CH2-OH +NaBr;
②甲苯与浓硝酸、浓硫酸混合加热发生取代反应,产生三硝基甲苯及水,所以实验室制备TNT的方程式为:![]() +3HNO3(浓)
+3HNO3(浓) ![]()
 +3H2O。
+3H2O。

【题目】纳米材料一直是人们研究的重要课题,例如纳米级Fe粉表面积大,具有超强的磁性,高效催化性等优良的性质。
I、实验室采用气相还原法制备纳米级Fe,其流程如图所示:
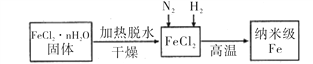
(1)纳米级Fe和稀盐酸反应的离子方程式为_______________________________。
(2)如何将FeCl2·nH2O固体加热脱水制得无水FeCl2 _____________________________________(用简要文字描述)。
(3)生成纳米级Fe的化学方程式为______________________________________。
II、查阅资料:在不同温度下,纳米级Fe粉与水蒸气反应的固体产物不同,温度低于570℃时生成FeO,高于570℃时生成Fe3O4。甲同学用如图甲装置所示进行纳米级Fe粉与水蒸气反应的实验,乙同学用图乙所示的装置进行纳米级Fe粉与水蒸气的反应并验证产物。

(4)甲装置中纳米级Fe粉与水蒸气反应的化学方程式是 ______________________。
(5)甲装置中仪器a的名称为_______________________。
(6)乙同学为探究实验结束后试管内的固体物质成分,进行了下列实验:
实验步骤 | 实验操作 | 实验现象 |
I | 将反应后得到的黑色粉末X(假定为均匀的),取出少量放入另一试管中,加入少量盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
II | 向实验I得到的溶液中滴加几滴KSCN溶液,振荡 | 溶液没有出现红色 |
根据以上实验,乙同学认为该条件下反应的固体产物为FeO。
丙同学认为乙同学的结论不正确,他的理由是______(用简要文字描述)。
(7)丁同学称取5.60gFe粉,用乙装反应一段时间后,停止加热。将试管内的固体物质在干燥器中冷却后,称得质量为6.88g,则丁同学实验后的固体物质中氧化物的质量分数为________(结果保留三位有效数字)。