题目内容
| |||||||||||||||||||||||||||||||||||
答案:6.AD;
解析:
解析:
(1) |
漏斗;玻璃棒(各1分,共2分) |
(2) |
在②步后的上层清液中,再滴入BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量(其它合理答案也可)2分 |
(3) |
NaOH、BaCl2、Na2CO3或BaCl2、Na2CO3、NaOH(2分) |
(4) |
在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度(2分) |
(5) |
未用玻璃棒引流;未用200 mL容量瓶.2分 |
(6) |
各1分,共2分多选、错选不得分 |

练习册系列答案
相关题目
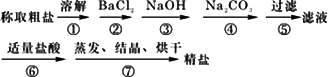


 为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):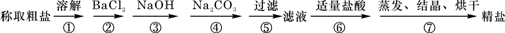

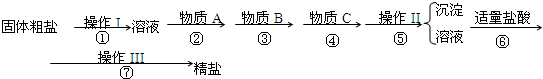
 aOH溶液 b、KOH溶液 c、BaCl2溶液 d、Ba(NO3)2溶液
aOH溶液 b、KOH溶液 c、BaCl2溶液 d、Ba(NO3)2溶液