题目内容
【题目】目前世界上60%的镁是从海水中提取的。海水提镁的主要流程如下:
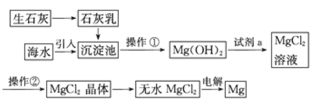
提示:①MgCl2晶体的化学式为MgCl2·6H2O。
②MgO的熔点为2852℃,无水MgCl2的熔点为714℃。
(1)操作①的名称是______,操作②的名称______、_____、过滤。
(2)试剂a的名称是_____。
(3)用氯化镁电解生产金属镁的化学方程式为______。
【答案】过滤 蒸发浓缩 冷却(或降温)结晶 盐酸 MgCl2(熔融)![]() Mg+Cl2↑
Mg+Cl2↑
【解析】
(1)分离不溶于水的固体和液体,可用过滤的方法,故操作①的名称是过滤;从沉淀池中得到氢氧化镁用过滤的方法,从氯化镁溶液中得到六水合氯化镁,可以通过蒸发浓缩或冷却结晶的方法获得六水合氯化镁,操作②的名称蒸发浓缩、冷却(或降温)结晶;
故答案为:过滤;蒸发浓缩 冷却结晶(或降温结晶);
(2)从氢氧化镁变为氯化镁,可以采用氢氧化镁和盐酸反应得到,反应的化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O,加入的足量试剂a是HCl,故试剂a的名称是盐酸,故答案为:盐酸;
(3)由于氧化镁的熔点高,熔融需要较多的能量,成本较高,而氯化镁的熔点较低,所以工业上冶炼镁的方法是电解熔融的MgCl2,通电后阳极氯离子失去电子生成氯气,阴极镁离子得到电子生成镁单质,故反应方程式为:MgCl2(熔融)![]() Mg+Cl2↑;
Mg+Cl2↑;
故答案为:MgCl2(熔融)![]() Mg+Cl2↑。
Mg+Cl2↑。

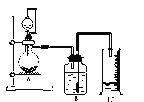
【题目】已知:KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O。如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是

选项 | 实验现象 | 结论 |
A | 滴有KSCN的FeCl2溶液变红 | Cl2具有还原性 |
B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
C | 紫色石蕊溶液先变红后褪色 | Cl2具有漂白性 |
D | KI淀粉溶液变蓝色 | Cl2具有氧化性 |