题目内容
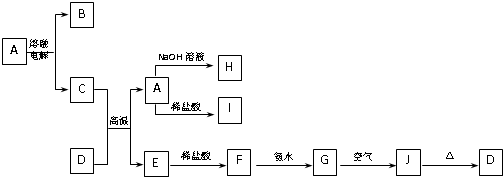
(10分)A—J是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已略去)。已知A是一种高熔点物质,D是一种红棕色固体。

请回答下列问题:做无机推断题找到突破点是关键,A是一种高熔点物质,可知A为Al2O3,D是一种红棕色固体,可知D为Fe2O3,B为O2,C为Al,E为Fe,F为FeCl2,G为Fe(OH)2,J为Fe(OH)3,H为NaAlO2,I为AlCl3。
(1)电解A物质的阳极电极反应式为___________,C与D在高温下反应,引发该反应需要加入的一种试剂是____________________(写化学式)
(2)写出G→J反应的实验现象与化学方程式____________________________________,__________________________________
(3)H 与I反应的离子方程式为___________________________________________
(4)用离子方程式表示I物质能用于净水的原理___________________________________
(1)2O2——4e—=O2 KClO3(各1分)
(2)生成的白色沉淀迅速变为灰绿色最终变为红褐色
4Fe(OH)2+O2+2H2O=4Fe(OH)3
(3)Al3++3AlO2—+6H2O=4Al(OH)3↓(4)Al3++ 3H2O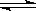 Al(OH)3(胶体)+ 3H+
Al(OH)3(胶体)+ 3H+
【解析】
试题分析:做无机推断题找到突破点是关键,A是一种高熔点物质,可知A为Al2O3,D是一种红棕色固体,可知D为Fe2O3,B为O2,C为Al,E为Fe,F为FeCl2,G为Fe(OH)2,J为Fe(OH)3,H为NaAlO2,I为AlCl3。
(1)阳极失去电子,电极反应式为2O2——4e—=O2。Al和Fe2O3反应需要引燃剂KClO3。
(2)Fe(OH)2→Fe(OH)3中发生的实验现象教材中很详细且常考的知识点,生成的白色沉淀迅速变为灰绿色最终变为红褐色,化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3。
(3)NaAlO2与AlCl3反应是双水解反应,离子方程式为:Al3++3AlO2—+6H2O=4Al(OH)3↓。
(4)AlCl3水解的原理是Al3+发生水解生成Al(OH)3(胶体)具有吸附能力,离子方程式为:Al3++ 3H2O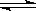 Al(OH)3(胶体)+ 3H+。
Al(OH)3(胶体)+ 3H+。
考点:无机物的推断
点评:本题考查了物质转化关系的应用,物质性质的应用,主要是铁及其化合物性质铝及其化合物性质的综合应用,关键是反应现象和反应条件的应用判断,特征反应的分析判断。

 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
 Fe(OH)3+3H+
Fe(OH)3+3H+

