题目内容
2.向恒温、恒容(2L)的密闭容器中充入2mol X和一定量的Y,发生反应:2X(g)+Y(g)$?_{△}^{催化剂}$2Z(g)△H=-197.74kJ/mol),4min后达到平衡,这时c(X)=0.2mol•L-1,且X与Y的转化率相等.下列说法中不正确的是( )| A. | 达到平衡时,再充入1molX,该反应的△H变大 | |
| B. | 用Y表示4min内的反应速率为0.1mol/(L•min) | |
| C. | 再向容器中充入1molZ,达到新平衡,n(X):n(Y)=2:1 | |
| D. | 4min后,若升高温度,平衡将向逆反应方向移动,平衡常数K减小 |
分析 A.热化学方程式中的焓变与化学计量数有关,与参加反应的反应物的物质的量无关;
B.根据v=$\frac{△c}{△t}$计算v(X),再利用速率之比等于化学计量数之比计算v(Y);
C.原平衡时X与Y的转化率相等,说明X、Y的起始物质的量之比等于化学计量数之比2:1,再向容器中充入1molZ,平衡向逆反应方向移动,反应过程中X、Y的物质的量之比为2:1,达新平衡时X、Y的物质的量之比不变;
D.升高温度,平衡向逆反应方向移动.
解答 解:A.热化学方程式中的焓变与化学计量数有关,与参加反应的反应物的物质的量无关,再充入1molX,平衡向正反应方向移动,但应热化学方程式中的焓变保持不变,故A错误;
B.v(X)=$\frac{\frac{2mol}{2L}-0.2mol/L}{4min}$=0.2mol•L-1•min-1,速率之比等于化学计量数之比,则v(Y)=$\frac{1}{2}$v(X)=0.1mol•L-1•min-1,故B正确;
C.原平衡时X与Y的转化率相等,说明X、Y的起始物质的量之比等于化学计量数之比2:1,再向容器中充入1molZ,平衡向逆反应方向移动,反应过程中X、Y的物质的量之比为2:1,达新平衡时X、Y的物质的量之比不变为2:1,故达到新平衡,c(X):c(Y)=2:1,故C正确;
D.该反应正反应是放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小,故D正确;
故选:A.
点评 本题考查化学平衡计算、化学平衡常数等,难度中等,注意反应物的起始物质的量之比等于化学计量数之比则转化率相等.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
19.2010年新春,北京一号地铁的车厢中都换上了“金施尔康”的广告,宣称它含有抗氧化成分,因此具有防止人体衰老的功能.人体血红蛋白中含有Fe2+,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+转变为Fe3+,生成高铁血红蛋白而丧失与O2结合的能力.服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C与“金施尔康”具有的性质是( )
| A. | 维生素C与“金施尔康”都是氧化剂 | |
| B. | 维生素C与“金施尔康”都是还原剂 | |
| C. | 维生素C是氧化剂,“金施尔康”是还原剂 | |
| D. | 维生素C是还原剂,“金施尔康”是氧化剂 |
20.下列反应:8NH3+3Cl2═6NH4Cl+N2,氧化剂和还原剂的物质的量之比是( )
| A. | 8:3 | B. | 3:6 | C. | 3:2 | D. | 3:8 |
17.为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气.下列关于Na2O2的叙述正确的是( )
| A. | Na2O2中阴、阳离子的个数比为1:1 | |
| B. | Na202比Na2O稳定,保存时可直接露置于空气中 | |
| C. | Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等 | |
| D. | Na2O2分别与水及CO2反应产生相同量的O2时,转移电子的物质的量相等 |
7.在可逆反应2A(g)+3B(g)?xC(g)+yD(g)中,已知起始浓度A为5mol/L,B为3mo1/L,C的反应速率为0.5mol/(L•min),反应开始达到平衡需2min,平衡时D的浓度为0.5mol/L.关于此反应下列说法中正确的是( )
| A. | A和B的平衡浓度之比为5:3 | B. | A和B的平衡浓度之比为2:3 | ||
| C. | x=1 | D. | x:y=2:1 |
12.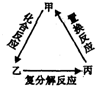 不能实现如图转化的单质甲是( )
不能实现如图转化的单质甲是( )
 不能实现如图转化的单质甲是( )
不能实现如图转化的单质甲是( )| A. | Si | B. | S | C. | Fe | D. | Cu |
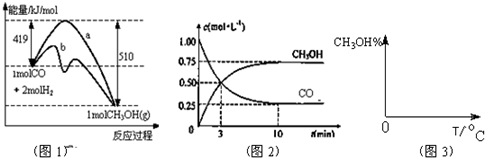
 常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题:
常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题: