题目内容
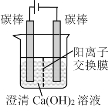
【题目】锂/氟化碳电池稳定性很高。电解质为LiClO4的二甲醚溶液,总反应为xLi+CFx=xLiF+C,放电产物LiF沉积在正极,工作原理如图所示。下列说法正确的是( )
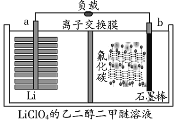
A.交换膜为阴离子交换膜
B.正极的电极反应式为CFx+xe-+xLi+=xLiF+C
C.电解质溶液可用LiClO4的乙醇溶液代替
D.a极电势高于b极电势
【答案】B
【解析】
A.Li+通过离子交换膜在正极上形成LiF,所以交换膜为阳离子交换膜,A错误;
B.石墨为正极,在正极上附着的CFx得电子生成LiF和C,正极的电极反应式为CFx+xe-+xLi+=xLiF+C,B正确;
C.金属Li是活泼金属,能与乙醇反应,所以不能用乙醇溶液代替,C错误;
D.由于Li活动性比石墨强,所以a为负极,b为正极,正极b极电势高于负极a电极的电势,D错误;
故合理选项是B。

练习册系列答案
相关题目
【题目】某研究小组在电压为24V时进行如下实验,电解3分钟后,发现下列现象。
编号 | ① | ② | ③ |
装置 |
|
|
|
现象 | 小灯泡微弱发光,两极均产生气泡,阳极附近出现白色浑浊,阴极附近无明显变化 | 两极均产生气泡,溶液无明显变化 | 两极均产生气泡,阳极附近出现白色浑浊,阴极附近无明显变化 |
下列说法正确的是( )
A.①中小灯泡微亮是因为Ca(OH)2是弱电解质
B.对比①和②,白色浑浊的出现与电极材料无关
C.对比①和③,白色浑浊是由于OH-迁移到阳极使Ca(OH)2沉淀析出
D.阳极附近白色沉淀的成分可能是CaCO3