题目内容
2.已知反应A(g)+3B(g)?2C(g)+2D(g),下列反应速率最快的是( )| A. | v(D)=0.3 mol•L-1•s-1 | B. | v (C)=0.4 mol•L-1•s-1 | ||
| C. | v (B)=0.6 mol•L-1•s-1 | D. | v (A)=0.25 mol•L-1•s-1 |
分析 不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,注意单位保持一致.
解答 解:不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,对应可逆反应:A+3B?2C+2D,
A.VD=0.3 mol•L-1•s-1,则$\frac{v{\;}_{D}}{2}$=0.15mol/(L•s);
B.$\frac{v{\;}_{C}}{2}$=0.2mol/(L•s);
C.$\frac{v{\;}_{B}}{3}$=0.2mol/(L•s);
D.vA=0.25 mol•L-1•s-1
故反应速率vA>vC=vB>D,
故选D.
点评 本题考查化学反应速率快慢比较,难度不大,利用比值法可以快速判断,也可以转化为同一物质表示的速率进行比较.

练习册系列答案
相关题目
12.下列说法正确的是( )
| A. | 1mol H2的体积为22.4L | |
| B. | 阿伏加德罗常数为6.02×1023 | |
| C. | Na+的摩尔质量为23 g/mol | |
| D. | 摩尔质量等于该粒子的相对原子质量或相对分子质量 |
10.甲苯分子被相对质量量为43的烷基取代苯环上一个H原子后,可能得到的产物有几种( )
| A. | 8 | B. | 6 | C. | 4 | D. | 3 |
7.恒温、恒容条件下,下列情况能说明反应N2(g)+3H2(g)?2NH3(g)达到化学平衡的是( )
| A. | 体系压强不再变化 | B. | v正(N2)=v逆(NH3) | ||
| C. | 反应体系密度不变 | D. | 反应体系中c(N2)=c(H2)=c(NH3) |
14.下列物质沸点最高的是( )
| A. | 乙烷 | B. | 丙烷 | C. | 正戊烷 | D. | 异戊烷 |
12.下列对氧化还原反应的分析中不合理的是( )
| A. | Mg变为MgO时化合价升高,故Mg在该反应中作还原剂 | |
| B. | 在反应2H2S+SO2═3S+2H2O中,氧化产物和还原产物都是S | |
| C. | 凡是氧化还原反应都有利于生产、生活 | |
| D. | 在反应2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑中,H2O既是还原剂又是氧化剂 |
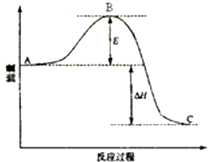 对于反应2SO2(g)+O2(g)?2SO3(g),反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.
对于反应2SO2(g)+O2(g)?2SO3(g),反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.