题目内容
7.两种气态烃组成的混合体0.1mol,完全燃烧得到0.16molCO2和3.6g水,下列说法错误的是( )| A. | 混合气体中一定有甲烷 | B. | 混合气体中可能是甲烷和乙烷 | ||
| C. | 混合气体中一定没有丙烷 | D. | 混合气体中可能有乙烯 |
分析 3.6g水的物质的量为:$\frac{3.6g}{18g/mol}$=0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,根据元素守恒,则混合烃的平均分子式为C1.6H4,而碳原子数小于1.6的只有甲烷,判断混合气体中一定含有甲烷,根据氢原子平均数目可知另一种烃分子中一定含有4个H原子,结合选项判断.
解答 解:3.6g水的物质的量为:$\frac{3.6g}{18g/mol}$=0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,根据元素守恒,则混合烃的平均分子式为C1.6H4,而碳原子数小于1.6的只有甲烷,判断混合气体中一定含有甲烷,根据氢原子平均数目可知另一种烃分子中一定含有4个H原子,可能为乙烯、丙炔等,一定不可能为乙烷、丙烷,故ACD正确,B错误,故选B.
点评 本题考查有机物分子式的确定,涉及混合烃组成的判断,难度中等,注意根据平均分子式进行判断,侧重考查学生分析解决问题的能力.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
18.下列过程中主要为化学能转化为热能的是( )
| A. |  木柴燃烧 | B. |  光合作用 | C. |  电解冶炼铝 | D. |  风力发电 |
15.下列现象与氢键有关的是( )
①NH3的熔、沸点比第ⅤA族其他元素氢化物的熔、沸点高
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④浓的氢氟酸溶液中存在HF2-和H2F3-
⑤水和乙醇分别与金属钠反应,前者比后者剧烈
⑥水分子在较高温度下也很稳定.
①NH3的熔、沸点比第ⅤA族其他元素氢化物的熔、沸点高
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④浓的氢氟酸溶液中存在HF2-和H2F3-
⑤水和乙醇分别与金属钠反应,前者比后者剧烈
⑥水分子在较高温度下也很稳定.
| A. | ①④⑤⑥ | B. | ①②③④ | C. | ①②③⑤ | D. | ①②③⑥ |
2.下列化学用语使用正确的是( )
| A. | 氢氧化钠的电子式: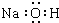 | B. | 甲烷的比例模型: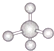 | ||
| C. | 只含有一个中子的氦原子:${\;}_{2}^{3}$He | D. | 乙醇的结构式:C2H5OH |
7.下列物质的水溶液因水解显酸性的是( )
| A. | NH4Cl | B. | NaClO | C. | CH3COOH | D. | K2SO4 |
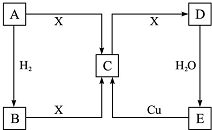 已知A是单质,A、B、C、D、E 5种物质均含同一种元素,X是地壳中含量最多的元素形成的单质,它们的相互转化关系如图所示.试回答下列问题.
已知A是单质,A、B、C、D、E 5种物质均含同一种元素,X是地壳中含量最多的元素形成的单质,它们的相互转化关系如图所示.试回答下列问题. ,结构简式H2C=CH2.
,结构简式H2C=CH2.