��Ŀ����
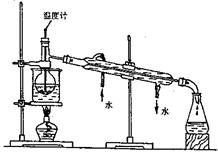
������ʾ��þ�뱥��̼��������Һ��Ӧ������������Ͱ�ɫ�����ijͬѧ���������ʵ�鷽������֤���̽����Ӧԭ����
��1���������
ʵ��I����ɰֽ��ȥþ����������Ĥ���������ʢ���������з�̪�ı���̼��������Һ���Թ��У�Ѹ�ٷ�Ӧ�������������ݺͰ�ɫ�������Һ��dz���졣
��ͬѧ�Է�Ӧ�в����İ�ɫ�������������²²⣺
�²�1����ɫ���������Ϊ ��
�²�2����ɫ���������ΪMgCO3��
�²�3����ɫ����������Ǽ�ʽ̼��þ[xMgCO3��yMg(OH)2]��
��2����ƶ���ʵ��ȷ�����ﲢ��֤�²⣺
| ʵ����� | ʵ�� | ʵ������ | ���� |
| ʵ��� | ��ʵ��I���ռ����������ȼ | �ܰ���ȼ�ա���������ɫ���� | ����ɷ�Ϊ___?___ |
| ʵ��� | ȡʵ��I�еİ�ɫ�����ϴ�ӣ��������� ? | ? | ��ɫ��������ܺ���MgCO3 |
| ʵ��� | ȡʵ��I�еij���Һ�������м�������CaCl2ϡ��Һ | ������ɫ���� | ��Һ�д��� �� ���� |

��ȡʵ��������ø�������İ�ɫ������22.6 g����ּ��������ٲ�������Ϊֹ����ʹ�ֽ����������ȫ������װ��A��B�С�ʵ��ǰ��װ��A����1.8 g��װ��B����8.8 g����ȷ����ɫ������Ļ�ѧʽ ��
��4�����ϻ�ѧ����ͻ�ѧƽ���ƶ�ԭ������Mg��NaHCO3��Һ��Ӧ�����������ݵ�ԭ��_________��
����9�֣�
��1���²�1��Mg(OH)2��1�֣�
��2�������� ����ϡ���ᣨ�������ɣ���
�۲������ݣ�����ȫ���ܽ� ����CO2- 3����1�֣�
��3�� 2MgCO3��Mg(OH)2 �� Mg(OH)2��2MgCO3 �� Mg3(OH)2(CO3)2
��4��NaHCO3��Һ�д�������ƽ�⣺HCO- 3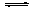 H+ +CO2- 3��H2O
H+ +CO2- 3��H2O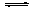 H++OH-��Mg��H+��Ӧ����H2��Mg2+��Mg2+��OH-��CO32-����������Mg(OH)2��2MgCO3����H+��OH-��CO2- 3��Ũ�Ⱦ����ͣ���ʹ������ƽ��������ƶ�����Mg�ͱ���NaHCO3��Һ��Ӧ������������H2��
H++OH-��Mg��H+��Ӧ����H2��Mg2+��Mg2+��OH-��CO32-����������Mg(OH)2��2MgCO3����H+��OH-��CO2- 3��Ũ�Ⱦ����ͣ���ʹ������ƽ��������ƶ�����Mg�ͱ���NaHCO3��Һ��Ӧ������������H2��
�������������
��1�������֪�²�ΪMg(OH)2
��2����þ��ˮ��Ӧ�����������ڼ��̼����һ��������ᡣ�ۿ��Ƿ��ж�����̼���ɡ�����Һ����CO32-��Ca2+���ɰ�ɫ������
��3����������ɵù�ϵʽMg(OH)2~H2O��MgCO3~CO2��n(H2O)=1.8g/18g/mol=0.1mol��n(CO2)=8.8g/44g/mol=0.2mol����֪Ϊ2MgCO3��Mg(OH)2 �� Mg(OH)2��2MgCO3 ��Mg3(OH)2(CO3)2 ��
��4��NaHCO3��Һ�д�������ƽ�⣺HCO- 3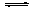 H+ +CO2- 3��H2O
H+ +CO2- 3��H2O H++OH-��Mg��H+��Ӧ����H2��Mg2+��Mg2+��OH-��CO32-����������Mg(OH)2��2MgCO3����H+��OH-��CO2- 3��Ũ�Ⱦ����ͣ���ʹ������ƽ��������ƶ�����Mg�ͱ���NaHCO3��Һ��Ӧ������������H2��
H++OH-��Mg��H+��Ӧ����H2��Mg2+��Mg2+��OH-��CO32-����������Mg(OH)2��2MgCO3����H+��OH-��CO2- 3��Ũ�Ⱦ����ͣ���ʹ������ƽ��������ƶ�����Mg�ͱ���NaHCO3��Һ��Ӧ������������H2��
���㣺������ʵ��̽��Ϊ���忼��Ԫ�ؼ��仯�������ʡ���ѧ��������֪ʶ����

 ��ٽ������½������������ϵ�д�
��ٽ������½������������ϵ�д���ҵ�ϳ�����ұ��п�����е�п������ZnO��FeO��Fe2O3��CuO��Al2O3�����ʣ�������������Zn(NO3)2��6H2O���壬�乤������Ϊ��
�й��������↑ʼ�����ͳ�����ȫ��pH���±���
| �������� | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| ��ʼ������pH | 3.3 | 1.5 | 6.5 | 4.2 | 5.4 |
| ������ȫ��pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.0 |
��1���ڡ�����������У�Ϊ���п�Ľ������ʣ���ͨ����������衱�⣬���ɲ�ȡ�Ĵ�ʩ�� ��
��2���ڡ�����I�������У����ټ�������H2O2��Һ��Ŀ���ǽ�Fe2+����Ϊ �����ڵ�����Һ��pHʹ��Ԫ��ת��Ϊ�������������ȥ��ΪʹFe(OH)3��Al(OH)3������ȫ����Zn(OH)2��������Ӧ������Һ��pH��ΧΪ �� ������Fe3+�Ƿ������ȫ��ʵ������Ǿ���Ƭ�̣�ȡ�����ϲ���Һ���μ� ��Һ����������Ѫ��ɫ������Fe3+������ȫ��
��3������Zn�۵������dz�ȥ��Һ�е� ��
CuSO4��Һ��Na2CO3��Һ��ϲ�������ɫ������������ij��ȤС��Գ�����ɵ�̽����
��������衿
����1������ΪCu (OH)2
����2������Ϊ
����3������Ϊ��ʽ̼��ͭ[��ѧʽ�ɱ�ʾΪnCuCO3��mCu (OH)2]
���������ϡ���������һ�ֳ������Ⱦ��ֽ⣨����������ᾧˮ����
������̽����
����1������������Һ���ˣ�������ˮϴ�ӣ�������ˮ�Ҵ�ϴ�ӣ���ɣ�
����2����ͬѧȡһ�������壬�����������õ�����װ�ã��г�����δ���������ж���ʵ�飻
��1������Ӧ��A������ɫ�����ڣ�C������������֤������ ������
��2����ͬѧ��ΪֻҪ����ͼ��Bװ�õ��Լ���������ij�Լ������֤�������м��裬���Լ��� ������ţ���
a��Ũ���� b����ˮCuSO4 c����ʯ�� d��P2O5
��3����ͬѧ����B�Լ�����֤����3������ʵ�������� ��
������̽����
��4����ͬѧ��һ��̽������3�й������ɣ�
����ͬѧ���һЩ������20������ݣ����±�����C�еij���ʯ��ˮ��ΪBa(OH)2��Һ����ԭ���� ��˫ѡ������ţ�
| �ܽ��(S)/g | �ܶȻ�(Ksp) | Ħ������(M)/g��mol��1 | |||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9��10-9 | 2.6��10-9 | 100 | 197 |
b��Ba(OH)2Ϊǿ�Ca(OH)2Ϊ����
c�����յ���CO2���ɵ�BaCO3����������CaCO3���������С
d����ͬ�����£�CaCO3���ܽ�����Դ���BaCO3
������ȡ����ɫ��������Ϊ54.2 g��ʵ�������װ��B����������5.4 g��C�еIJ�������������Ϊ39.4 g���������ɫ����Ļ�ѧʽΪ ��
ijУ��ѧС���ͬѧ������̼��Ϊ�缫����Ȼ�ͭ��Һʱ��������̼���ϳ����к�ɫ���������⣬����������ɫ����������Ϊ̽������̼���ϵIJ����������¹��̣�
�������
ͭ�Ļ�������ɫ�������£�
| ���� | ��ɫ������ | ���� | ��ɫ������ |
| ������ͭCu(OH)2 | ��ɫ���岻����ˮ | ����ͭ��CuSO4�� | ��Һ����ɫ |
| ������ͭ��CuO�� | ��ɫ���岻����ˮ | �Ȼ�ͭ��CuCl2�� | ��Һ����ɫ��ϡ��Һ����ɫ |
| �Ȼ���ͭ��CuCl�� | ��ɫ���岻����ˮ | ��ʽ�Ȼ�ͭ | ��ɫ���岻����ˮ |
��1��������裺�ٺ�ɫ����һ����ͭ����������Cu2O���ڰ�ɫ����Ϊͭ�Ļ�����仯ѧʽ����ΪCuCl
��2��ʵ����֤��ȡ���CuCl2��Һ�������̼����ϴ�ӡ������������װ�ý���ʵ�飬��֤��������

ʵ�������̼���ϵİ�ɫ���ʱ�Ϊ��ɫ����ˮ����ͭ����ɫ��
��̼���ϵĺ�ɫ�����Ƿ���Cu2O ����ǡ�����������
������cװ�ú�����ͨ�� �У������ְ�ɫ��������˵�����������еİ�ɫ����һ�����ڣ���д��װ��b�з�����Ӧ�Ļ�ѧ����ʽ��
��
��3���������ۣ�
�ٵ��CuCl2��Һ��������Ϸ����ķ�ӦΪ��Cu2++2e-��Cu�� ������ʯī�缫��ⱥ������ͭ��Һ���۲�����̼��������ֵ������ɫ���ʸ��ţ��ް�ɫ���ʣ����� �������⣬���ְ�ɫ���ʡ�
Ҫ��װһ��ʵ��������Һ���Һ�巴Ӧ�Ʊ������װ�ã�����������µ��岽��������ȷ�ij�����
�ٽ�������ƿ�̶�������̨��
�ڽ��ƾ��Ʒ�������̨�ϣ����ݾƾ���ȷ����Ȧ�߶ȣ��̶���Ȧ���ź�ʯ����
����©����������ƿ�м���һ��Һ�巴Ӧ������Һ©���м�����һ��Һ�巴Ӧ����������ܷ��������ռ�װ����
�ܼ��װ�õ�������(���ù̶�װ���ȵķ������������)
����������ƿ��װ�÷�Һ©�������Ӻõ�����
| A���ڢ٢ݢܢ� | B���ܢڢ٢ݢ� |
| C���ڢ٢ݢۢ� | D���٢ݢܢڢ� |