题目内容
【题目】某无色溶液中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 这几种离子中的若干种,依次进行下列实验,观察到的现象记录如下:①
这几种离子中的若干种,依次进行下列实验,观察到的现象记录如下:①![]() 试纸检验,溶液的
试纸检验,溶液的![]() ②取少量原溶液,向溶液中加入过量的
②取少量原溶液,向溶液中加入过量的![]() 和盐酸的混合溶液,无白色沉淀生成③另取少量原溶液,向溶液中滴加足量氯水、无气体产生,再加入
和盐酸的混合溶液,无白色沉淀生成③另取少量原溶液,向溶液中滴加足量氯水、无气体产生,再加入![]() 振荡,静置后
振荡,静置后![]() 层呈橙色,用分液漏斗分液④向分液后的水溶液中加入
层呈橙色,用分液漏斗分液④向分液后的水溶液中加入![]() 和
和![]() 溶液,有白色沉淀产生⑤在滤液中加入
溶液,有白色沉淀产生⑤在滤液中加入![]() 和
和![]() 的混合溶液有白色沉淀产生。则关于原溶液的判断中正确的是
的混合溶液有白色沉淀产生。则关于原溶液的判断中正确的是
A.肯定不存在的离子是![]() 、
、![]() 、
、![]() 、
、![]()
B.肯定存在的离子是![]() 、
、![]() 、
、![]()
C.无法确定原溶液中是否存在![]() 和
和![]()
D.若步骤④改用![]() 和盐酸的混合溶液,则对溶液中离子的判断也无影响
和盐酸的混合溶液,则对溶液中离子的判断也无影响
【答案】D
【解析】
无色溶液中一定不存在有色离子:![]() 、
、![]() ;
;
![]() 试纸检验,溶液呈碱性,说明溶液中存在弱酸根离子
试纸检验,溶液呈碱性,说明溶液中存在弱酸根离子![]() 或
或![]() ;
;
![]() 取少量原溶液,向溶液中加入过量的
取少量原溶液,向溶液中加入过量的![]() 和盐酸的混合溶液,无白色沉淀生成,硫酸钡不溶于盐酸,说明溶液中一定不存在
和盐酸的混合溶液,无白色沉淀生成,硫酸钡不溶于盐酸,说明溶液中一定不存在![]() ;
;
![]() 另取少量原溶液,向溶液中滴加足量氯水,无气体产生,说明没有
另取少量原溶液,向溶液中滴加足量氯水,无气体产生,说明没有![]() ,再加入
,再加入![]() 振荡,静置后
振荡,静置后![]() 层呈橙红色,橙色物质为溴单质,说明溶液中一定存在
层呈橙红色,橙色物质为溴单质,说明溶液中一定存在![]() ;
;
![]() 用分液漏斗分液,取上层溶液,加入
用分液漏斗分液,取上层溶液,加入![]() 和
和![]() 溶液有白色沉淀产生,说明有硫酸钡生成,即含有
溶液有白色沉淀产生,说明有硫酸钡生成,即含有![]() ,
,
![]() 在滤液中加入
在滤液中加入![]() 和
和![]() 的混合溶液有白色沉淀产生,由于
的混合溶液有白色沉淀产生,由于![]() 加入氯水引进了氯离子,无法证明原溶液中是否存在氯离子;
加入氯水引进了氯离子,无法证明原溶液中是否存在氯离子;
由电荷守恒可知溶液中还一定含有![]() ;
;
根据以上分析可知,原溶液中一定存在的离子为:![]() 、
、![]() 、
、![]() ,一定不存在的离子为:
,一定不存在的离子为:![]() 、
、![]() 、
、![]() 、
、![]() ,无法确定的离子为:
,无法确定的离子为:![]() ,
,
A.根据分析可知,溶液中一定不存在的离子为:![]() 、
、![]() 、
、![]() 、
、![]() ,一定含有
,一定含有![]() 、
、![]() 、
、![]() ,故A错误;
,故A错误;
B.原溶液中一定不存在![]() ,故B错误;
,故B错误;
C.根据分析可知,溶液中一定不存在![]() ,故C错误;
,故C错误;
D.若步骤![]() 目的是检验是否含有
目的是检验是否含有![]() ,改用
,改用![]() 和盐酸的混合溶液,则对溶液中离子的判断也无影响,故D正确;
和盐酸的混合溶液,则对溶液中离子的判断也无影响,故D正确;
故答案为D。

【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10﹣4molL﹣1 | K1=4.4×10﹣6molL﹣1 K2=5.6×10﹣11molL﹣1 | 3.0×10﹣8 molL﹣1 |
请回答下列问题:
(1)同浓度的CH3COOH、H2CO3、HClO溶液的pH最大的是_____.
(2)常温下0.1molL﹣1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是_____(填字母序号,下同).
A.c(H+)
B.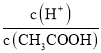
C.c(H+)c(OH﹣)
D.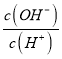
E.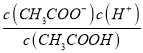
若该溶液升高温度,上述5种表达式的数据增大的是_________.
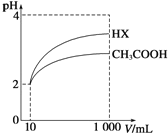
(3)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:则HX的电离平衡常数_____(填“大于”、“等于”或“小于”)醋酸的平衡常数.稀释后,HX溶液中有水电离出来的c(H+)_____(填“大于”、“等于”或“小于”)醋酸的溶液中有水电离出来的c(H+),理由是___________.
(4)已知100℃时,水的离子积为1×10﹣12,该温度下测得某溶液PH=7,该溶液显_____(填“酸”、“碱”或“中”)性.将此温度下PH=1的H2SO4溶液aL与PH=11的NaOH溶液bL混合,若所得混合液PH=2,则a:b=_____.
【题目】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,请填写下列空白:
(1)选用的指示剂是______________________。
(2)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视______________________。
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______________。
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(4)若滴定开始和结束时,酸式滴定管中的液面如图所示,请将数据填入下面表格的横线处。
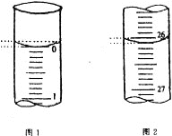
滴定次数 | 待测氢氧化钠溶液的体积/ mL | 0.1000 mol/L 盐酸的体积/ mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/ mL | ||
第一次 | 25.00 | 0.00 | ________ | _______ |
第二次 | 25.00 | 2.00 | 28.08 | 26.08 |
第三次 | 25.00 | 0.22 | 26.34 | 26.12 |
(5)请根据上表中数据列式计算该氢氧化钠溶液的物质的量浓度:c(NaOH)= _________。
(6)滴定终点的判定依据是_______________。