题目内容
【题目】已知:![]() (X为卤素原子);
(X为卤素原子);
Ⅱ.与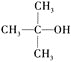 结构相似的醇不能被氧化成醛或酸。
结构相似的醇不能被氧化成醛或酸。
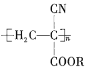
“智能型”大分子在生物工程中有广泛的应用前景,![]() 就是一种“智能型”大分子,可用于生物制药中大分子与小分子的分离。下图是以烃
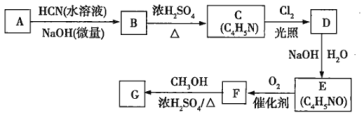
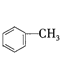
就是一种“智能型”大分子,可用于生物制药中大分子与小分子的分离。下图是以烃![]() 为起始反应物合成
为起始反应物合成![]() 的路线图:
的路线图:

根据上述过程回答下列问题:
(1)写出对应物质的结构简式:![]() _______________,
_______________,![]() _______________。
_______________。
(2)写出上述过程中所发生反应的反应类型:①____________,②_____________,③_________,④_________。
(3)写出反应③的化学方程式:_____________________。
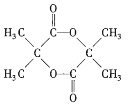
(4)![]() 在浓硫酸存在并加热的条件下反应还可能生成一种六元环状产物,该六元环状产物的结构简式为_____________________。
在浓硫酸存在并加热的条件下反应还可能生成一种六元环状产物,该六元环状产物的结构简式为_____________________。
(5)下列有关![]() 的说法正确的是___________(填序号)。
的说法正确的是___________(填序号)。
A.能够发生加成反应 B.能够发生酯化反应
C.不能燃烧 D.能够使酸性![]() 溶液褪色
溶液褪色
【答案】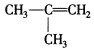
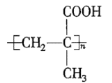 加成反应 取代反应 消去反应 加聚反应
加成反应 取代反应 消去反应 加聚反应 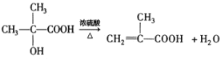
 B
B
【解析】
F含有碳碳双键,发生加聚反应生成高分子化合物PMAA,故PMAA为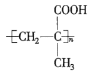 ,烃A与氯气反应得到B,结合信息Ⅰ知B发生卤代烃的水解反应生成C,C发生连续氧化反应生成E,E在浓硫酸、加热条件下反应生成F,E→F发生的是消去反应,故E中含有-OH、-COOH,且-OH连接的碳原子上没有氢原子,故E为
,烃A与氯气反应得到B,结合信息Ⅰ知B发生卤代烃的水解反应生成C,C发生连续氧化反应生成E,E在浓硫酸、加热条件下反应生成F,E→F发生的是消去反应,故E中含有-OH、-COOH,且-OH连接的碳原子上没有氢原子,故E为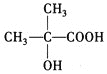 ,逆推可知D为
,逆推可知D为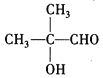 ,C为
,C为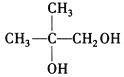 ,B为
,B为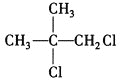 ,反应①为烯烃的加成反应,故A为
,反应①为烯烃的加成反应,故A为 。
。
(1)由上述分析可知,A的结构简式为 ,PMAA的结构简式为
,PMAA的结构简式为 ,故答案为:
,故答案为: ;
; ;
;
(2)反应①是 与氯气发生加成反应,反应②是卤代烃的水解反应,属于取代反应,反应③是醇的消去反应,反应④是碳碳双键发生加聚反应,故答案为:加成反应;取代反应;消去反应;加聚反应;
与氯气发生加成反应,反应②是卤代烃的水解反应,属于取代反应,反应③是醇的消去反应,反应④是碳碳双键发生加聚反应,故答案为:加成反应;取代反应;消去反应;加聚反应;
(3)反应③为醇的消去,方程式为 ,故答案为:
,故答案为: ;
;
(4)E( )在浓硫酸存在并加热的条件下-COOH和-OH能发生酯化反应生成环酯,该环状产物的结构简式是
)在浓硫酸存在并加热的条件下-COOH和-OH能发生酯化反应生成环酯,该环状产物的结构简式是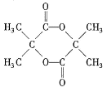 ,故答案为:
,故答案为: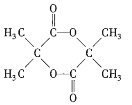 ;
;
(5)PMAA为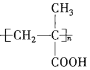 ,据此
,据此
A.该物质不含能发生加成反应的官能团,A错误;
B.有羧基,可发生酯化反应,B正确;
C.含![]() 三种元素,可以燃烧,C错误;
三种元素,可以燃烧,C错误;
D.不含碳碳双键、碳碳三键、醛基、羟基等能使酸性KMnO4溶液褪色的官能团;
故答案为:B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】工业上以锂辉石为原料生产碳酸锂的部分工业流程如下:

已知:
①锂辉石的主要成分为Li2O·Al2O3·4SiO2,其中含少量Ca、Mg元素。
②Li2O·Al2O3·4SiO2 + H2SO4(浓) ![]() Li2SO4 + Al2O3·4SiO2·H2O
Li2SO4 + Al2O3·4SiO2·H2O
③某些物质的溶解度(s)如下表所示。
T/℃ | 20 | 40 | 60 | 80 |
s(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
s(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(1)从滤渣Ⅰ中分离出Al2O3的流程如下图所示。请写出生成沉淀的离子方程式______。
![]()
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3。向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)________________________________________________。
(3)最后一个步骤中,用“热水洗涤”的原因是______________________________。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下:
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液做阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入少量NH4HCO3溶液并共热,过滤、烘干得高纯Li2CO3。
①a中,阳极的电极反应式是_________________________
②电解后,LiOH溶液浓度增大的原因_________________,b中生成Li2CO3反应的化学方程式是___________________________________________。
(5)磷酸亚铁锂电池总反应为:FePO4+Li![]() LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:__________________。
LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:__________________。
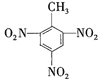
【题目】下表中Ⅱ对Ⅰ的解释不正确的是( )
选项 | Ⅰ | Ⅱ |
A | 2 | 苯环使羟基活泼 |
B |
| 羟基使苯环活泼 |
C |
| 苯环使羟基活泼 |
D |
| 甲基使苯环活泼 |
A.AB.BC.CD.D