题目内容
已知水在25℃和95℃时,其电离平衡曲线如图所示:(1)25°C时,水的电离平衡曲线应为哪一条?请说明理由______
(2)95°C时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为为多少?
(3)95°C时,若10体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是?
(4)曲线B对应的温度下,pH=2的某酸HA与pH=10的NaOH溶液等体积混合后,溶液的pH=5,请分析其原因______.
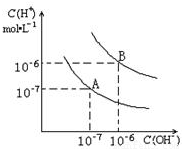
【答案】分析:(1)水的电离是吸热过程,降低温度抑制水电离,导致水中c(H+)、c(OH-)都减小;
(2)先根据温度和混合溶液pH大小确定溶液的酸碱性,根据溶液的pH计算酸和碱的体积之比;
(3)酸、碱都是强电解质,溶液呈中性说明氢离子和氢氧根离子的物质的量相等,结合水的离子积常数确定强酸的pH1与强碱的pH2之间应满足的关系;
(4)曲线B对应95℃,pH=2的某酸HA中氢离子浓度与pH=10的NaOH溶液中氢氧根离子浓度相等,HA若为强酸,完全反应后pH=6,实际上pH=5,说明酸过量,则该酸为弱酸.
解答:解:(1)水的电离是吸热过程,升高温度,使水的电离程度增大,当温度升高时,促进水的电离,水的离子积增大,水中氢离子、氢氧根离子浓度都增大,水的pH减小,但溶液仍然呈中性;
故答案为:A 水的电离是吸热过程,温度低时,电离程度小,c(H+)、c(OH-)小;
(2)95°C时纯水的pH=6,混合溶液的pH=7,说明酸、碱混合时碱过量溶液呈碱性,混合溶液中c(OH-)=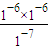 mol/L=10-5 mol/L,pH=9的NaOH溶液中c(OH-)=
mol/L=10-5 mol/L,pH=9的NaOH溶液中c(OH-)=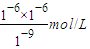 =10-3mol/L,
=10-3mol/L,
设酸的体积为x,碱的体积为y,c(OH-)=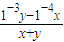 =10-5 mol/L,x:y=9:1;
=10-5 mol/L,x:y=9:1;
答:碱的体积必是酸的9倍;
(3)要注意的是95°C时,水的离子积为10-12,即酸、碱浓度相等时pH(酸)+pH(碱)=12.现强碱的OH-浓度是强酸H+浓度的10倍,所以pH(酸)+pH(碱)=13,即pH1+pH2=13,或a+b=13;
(4)曲线B对应95℃,pH=2的某酸HA中氢离子浓度与pH=10的NaOH溶液中氢氧根离子浓度相等,HA若为强酸,完全反应后pH=6,实际上pH=5,说明酸过量,则该酸为弱酸,HA中和NaOH后,混合溶液中还剩余较多的HA分子,可继续电离出H+,导致溶液中氢离子浓度大于氢氧根离子浓度而使溶液呈酸性;
故答案为:曲线B对应95℃,此时水的离子积为10-12,HA若为强酸,最后应为pH=6,现pH=5,说明HA为弱酸,HA中和NaOH后,混合溶液中还剩余较多的HA分子,可继续电离出H+.
点评:本题考查水的电离和酸、碱混合的pH计算问题,难度较大,注意温度不同而使水的离子积常数不同是解本题的关键,注意无论温度多高,纯水中始终氢离子浓度等于氢氧根离子浓度,呈中性,为易错点.
(2)先根据温度和混合溶液pH大小确定溶液的酸碱性,根据溶液的pH计算酸和碱的体积之比;
(3)酸、碱都是强电解质,溶液呈中性说明氢离子和氢氧根离子的物质的量相等,结合水的离子积常数确定强酸的pH1与强碱的pH2之间应满足的关系;
(4)曲线B对应95℃,pH=2的某酸HA中氢离子浓度与pH=10的NaOH溶液中氢氧根离子浓度相等,HA若为强酸,完全反应后pH=6,实际上pH=5,说明酸过量,则该酸为弱酸.
解答:解:(1)水的电离是吸热过程,升高温度,使水的电离程度增大,当温度升高时,促进水的电离,水的离子积增大,水中氢离子、氢氧根离子浓度都增大,水的pH减小,但溶液仍然呈中性;
故答案为:A 水的电离是吸热过程,温度低时,电离程度小,c(H+)、c(OH-)小;
(2)95°C时纯水的pH=6,混合溶液的pH=7,说明酸、碱混合时碱过量溶液呈碱性,混合溶液中c(OH-)=
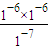 mol/L=10-5 mol/L,pH=9的NaOH溶液中c(OH-)=
mol/L=10-5 mol/L,pH=9的NaOH溶液中c(OH-)=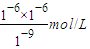 =10-3mol/L,
=10-3mol/L,设酸的体积为x,碱的体积为y,c(OH-)=
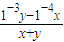 =10-5 mol/L,x:y=9:1;
=10-5 mol/L,x:y=9:1;答:碱的体积必是酸的9倍;
(3)要注意的是95°C时,水的离子积为10-12,即酸、碱浓度相等时pH(酸)+pH(碱)=12.现强碱的OH-浓度是强酸H+浓度的10倍,所以pH(酸)+pH(碱)=13,即pH1+pH2=13,或a+b=13;
(4)曲线B对应95℃,pH=2的某酸HA中氢离子浓度与pH=10的NaOH溶液中氢氧根离子浓度相等,HA若为强酸,完全反应后pH=6,实际上pH=5,说明酸过量,则该酸为弱酸,HA中和NaOH后,混合溶液中还剩余较多的HA分子,可继续电离出H+,导致溶液中氢离子浓度大于氢氧根离子浓度而使溶液呈酸性;
故答案为:曲线B对应95℃,此时水的离子积为10-12,HA若为强酸,最后应为pH=6,现pH=5,说明HA为弱酸,HA中和NaOH后,混合溶液中还剩余较多的HA分子,可继续电离出H+.
点评:本题考查水的电离和酸、碱混合的pH计算问题,难度较大,注意温度不同而使水的离子积常数不同是解本题的关键,注意无论温度多高,纯水中始终氢离子浓度等于氢氧根离子浓度,呈中性,为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
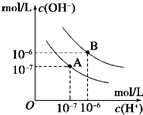 已知水在25℃和95℃时,其电离平衡曲线如图所示,下列说法错误的( )
已知水在25℃和95℃时,其电离平衡曲线如图所示,下列说法错误的( )| A、A曲线代表25℃时水的电离平衡曲线 | B、当95℃时,pH=6的溶液呈中性 | C、25℃时,将10mLpH=12的NaOH溶液与1mLpH=1的H2SO4溶液混合,所得溶液的pH=7 | D、95℃时,等体积等物质的量浓度的HA溶液和NaOH溶液混合后,当混合溶液的pH=6时,说明HA酸为弱酸 |
 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: (1)写出下列物质溶于水的电离方程式①冰醋酸溶于水:
(1)写出下列物质溶于水的电离方程式①冰醋酸溶于水: 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: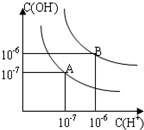 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: