题目内容
【题目】某兴趣活动小组利用物质间的互变,设计成一个平面魔方,如右图所示:
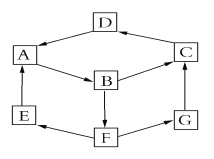
已知①A、B、C、D、G含有同种元素。
②
纯A(单质) | B溶液 | D固体 | G溶液 | |
颜色 | 银白色 | 黄色 | 红棕色 | 浅绿色 |
③E是通常情况下密度最小的气体;B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀,也能将一种氧化物氧化为F,F是含有三种元素的化合物,与A反应生成E、G。
依据以上信息填空:
(1)写出D的化学式: 。
(2)G生成C的过程中所出现的现象为 写出对应的离子方程式
(3)写出反应A→B的化学方程式: 。
(4)B→F的离子方程式为 ;G与次氯酸反应的离子方程式为 。
【答案】⑴Fe2O3 ;⑵先产生白色沉淀,迅速变为灰绿色,最后变为红褐色,Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4 Fe(OH)3;(3)2Fe+3Cl2![]() 2FeCl3;⑷ 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,2Fe2++2HClO=2Fe3++Cl-+ H2O+ClO-。
2FeCl3;⑷ 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,2Fe2++2HClO=2Fe3++Cl-+ H2O+ClO-。
【解析】
试题分析:(1)根据信息,D固体是红棕色,则D为Fe2O3;(2)G溶液为浅绿色,则G中含有Fe2+,C可以生成Fe2O3,推出C为Fe(OH)3,因此离子反应方程式为:Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4 Fe(OH)3,现象是:先产生白色沉淀,迅速变为灰绿色,最后变为红褐色;(3)因为五种物质都含有同种元素,且A为单质,银白色,则A为Fe,B溶液先黄色,说明含有Fe3+,B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀,推出B为含有Cl-,则B为FeCl3,2Fe+3Cl2![]() 2FeCl3;(4)E是通常情况下密度最小的气体,E为H2,F能和Fe反应生H2和Fe2+,且属于三种元素的化合物,则F为H2SO4,因此此氧化物是SO2,2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ ,利用次氯酸的强氧化性,把Fe2+氧化成Fe3+,即2Fe2++2HClO=2Fe3++Cl-+ H2O+ClO-。
2FeCl3;(4)E是通常情况下密度最小的气体,E为H2,F能和Fe反应生H2和Fe2+,且属于三种元素的化合物,则F为H2SO4,因此此氧化物是SO2,2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ ,利用次氯酸的强氧化性,把Fe2+氧化成Fe3+,即2Fe2++2HClO=2Fe3++Cl-+ H2O+ClO-。

 阅读快车系列答案
阅读快车系列答案