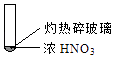��Ŀ����
����Ŀ��������ͼ��ʾ��װ���ռ�����4�����壺��NO2����NH3����NO����SO2 �� 
��1������ƿ�Ǹ���ģ�����B�ڽ��������ռ��������� �� ����A�ڽ��������ռ��������� ��
��2��������ƿ�ڳ���ˮ�����ռ��������� �� ����Ӧ���ڽ��룮
��3������ƿ��װ������Ũ���ᣬ���ܱ������������ �� ����Ӧ���ڽ��룮
��4���ڱ�״���£���NO�������������ƿ������ƿ������ˮ�У�����ƿ������ͨ��O2 �� ƿ��Һ��仯����� �� ������ƿ����Һ����ɢ��������ƿ����Һ�����ʵ����ʵ���Ũ��ΪmolL��1 ��
���𰸡�
��1���٢ܣ���
��2���ۣ� A
��3���ڣ� B
��4�������� ![]()
���������⣺��1����B�ڽ��������ռ��������ܶ�Ӧ�ô��ڿ����������������У���NO2����SO2��
����A�ڽ��������ռ������壬���൱�������ſ�������������ܶ�С�ڿ���������������Ϊ����NH3��
�ʴ�Ϊ���٢ܣ��ڣ���2��������ƿ�ڳ���ˮ�������ռ���ˮ��Ӧ��������ˮ�����壬�ܹ�������ˮ���ռ�������Ϊ����NO������Ӧ�ôӶ̵���A������Һ��ӳ�����B�ų���
�ʴ�Ϊ���ۣ�A����3��Ũ����Ϊ���Ը�������ܹ���Ũ���ᷴӦ�ļ������岻����Ũ��������ڰ�������������ʱ������Ӧ�ôӳ�����B������
�ʴ�Ϊ���ڣ�B����4���ڱ�״���£���NO�������������ƿ������ƿ������ˮ�У�����ƿ������ͨ��O2���ᷢ����Ӧ��4NO+2H2O+3O2=4HNO3������һ���������٣�ƿ��Һ���������
����ƿ���ݻ�ΪVL��������VLһ�����������ʵ���Ϊ��n��NO��= ![]() =
= ![]() mol�����ݵ�ԭ���غ㣬��Ӧ��������������ʵ���Ϊ��
mol�����ݵ�ԭ���غ㣬��Ӧ��������������ʵ���Ϊ�� ![]() mol����Ӧ����������ʵ���Ũ��Ϊ��
mol����Ӧ����������ʵ���Ũ��Ϊ�� ![]() =
= ![]() mol/L��
mol/L��
�ʴ�Ϊ�������� ![]() ��
��
��1����B��������Ϊ�����ſ������ռ���������ܶȴ��ڿ������ܶȣ���A������Ϊ�����ſ������������ܶ�С�ڿ�����ע�ⲻ��ʹ���ſ�����ˮ��NO����2����ˮ���ռ�����ʱ�����岻����ˮ��Ӧ����ˮ���ܽ�Ƚ�С���������������������������Ȳ���ʹ����ˮ���ռ�������Ӧ�ò��á��̽�������������3��Ũ����Ϊ���Ը���������ܸ���������壻��������ʱ������Ӧ�ôӳ����ܽ������̵��ܳ�������4������һ��������������ˮ�ķ�Ӧ����ʽ���з���Һ��仯�������ƿ���ݻ������ݵ�ԭ���غ�������Ӧ������������ʵ������ٸ������ʵ���Ũ�ȵĸ�������ϡ�͵����ʵ���Ũ�ȣ�

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�����Ŀ������ʵ���о��к���ɫ����������Աȷ������Ľ��۲���ȷ���ǣ�������
|
|
|
�� | �� | �� |
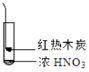
A.�ɢ��еĺ���ɫ���壬�ƶϲ���������һ���ǻ������
B.����ɫ���岻�ܱ�������ľ̿��Ũ��������˷�Ӧ
C.�ɢ�˵��Ũ������лӷ��ԣ����ɵĺ���ɫ����Ϊ��ԭ����
D.�۵���������м���CO2 �� �ɴ�˵��ľ̿һ����Ũ���ᷢ���˷�Ӧ