题目内容
【题目】著名化学家徐光宪获得国家最高科学技术奖,以表彰他在稀土萃取理论方面作出的贡献。已知:金属铈(稀土元素)在空气中易氧化变暗,受热时燃烧,遇水很快反应。(注:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+>I2。)下列说法正确的是
A. 铈溶于氢碘酸的化学方程式可表示为:Ce + 4HI![]() CeI4+ 2H2↑
CeI4+ 2H2↑
B. 用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4+ + 2Fe2+=Ce3++ 2Fe3+
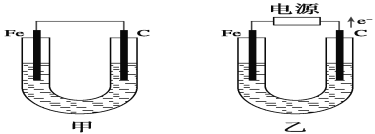
C. 在一定条件下,电解熔融状态的CeO2制Ce,在阴极获得铈
D. 铈的四种核素![]() 、
、![]() 、
、![]() 、
、![]() ,它们互称为同素异形体
,它们互称为同素异形体
【答案】C
【解析】
根据题中信息分析,根据电荷守恒判断,根据同位素及同素异形体的定义判断。
A.由于氧化性Ce4+>Fe3+>I﹣,铈溶于氢碘酸,产物不会生成CeI4,应该是CeI3,故A错误;
B.离子方程式中,Ce4++2Fe2+=Ce3++2Fe3+,左边总电荷为+8,右边总电荷为9,电荷不守恒,正确应为Ce4++Fe2+=Ce3++Fe3+,故B错误;
C. 电解熔融状态的CeO2制Ce,化合价降低发生还原反应,阴极发生还原反应,多以在阴极获得铈,故C正确;
D. 四种铈的核素![]()
![]() 、
、![]() 、
、![]() 、
、![]() ,具有相同质子数,不同中子数,故它们互为同位素,不是同素异形体,故D错误。
,具有相同质子数,不同中子数,故它们互为同位素,不是同素异形体,故D错误。
故选C。

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目