题目内容
【题目】实验室用如下装置(略去部分夹持装置)模拟利用氨气和次氯酸钠合成肼(N2H4)的过程。下列说法正确的是( )
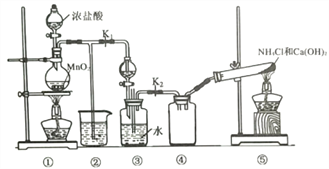
A. 将装置① 中浓盐酸换成H2O2,也可用于制备氧气 B. ②中盛装NaOH溶液,用于吸收多余的Cl2
C. ③分液漏斗中盛装饱和食盐水 D. 当反应结束时,④中可收集一瓶纯净的NH3
【答案】B
【解析】
由图可知,①中发生的反应为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,打开K1,Cl2能和NaOH溶液反应生成NaCl、NaClO,⑤用来制取NH3,④装置作安全瓶,能防倒吸,在③中氨气和NaClO反应生成N2H4,发生ClO-+2NH3=N2H4+Cl-+H2O,最后关闭K1,②中盛装NaOH溶液,用于吸收多余的Cl2。A.装置①中浓盐酸换成H2O2,制备氧气时不需要加热,二氧化锰作催化剂,故A错误;B.氯气有毒,不能排放在环境中,则②中盛装NaOH溶液,用于吸收多余的Cl2,故B正确;C.③分液漏斗中应该盛装NaOH溶液,利用氯气与NaOH溶液反应制备NaClO,故C错误;D.反应结束后,关闭K2,多余的氨气可收集在④中,但氨气中混有水蒸气,故D错误;故选B。
MnCl2+Cl2↑+2H2O,打开K1,Cl2能和NaOH溶液反应生成NaCl、NaClO,⑤用来制取NH3,④装置作安全瓶,能防倒吸,在③中氨气和NaClO反应生成N2H4,发生ClO-+2NH3=N2H4+Cl-+H2O,最后关闭K1,②中盛装NaOH溶液,用于吸收多余的Cl2。A.装置①中浓盐酸换成H2O2,制备氧气时不需要加热,二氧化锰作催化剂,故A错误;B.氯气有毒,不能排放在环境中,则②中盛装NaOH溶液,用于吸收多余的Cl2,故B正确;C.③分液漏斗中应该盛装NaOH溶液,利用氯气与NaOH溶液反应制备NaClO,故C错误;D.反应结束后,关闭K2,多余的氨气可收集在④中,但氨气中混有水蒸气,故D错误;故选B。

【题目】卤块的主要成分是MgCl2,此外还含有Fe3+、Fe2+和Mn2+等离子。若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁。
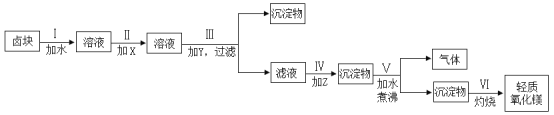
已知1:生成氢氧化物沉淀的pH
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)2 | 7.6 | 9.6 |
Fe(OH)3 | 2.7 | 3.7 |
Mn(OH)2 | 8.3 | 9.8 |
Mg(OH)2 | 9.6 | 11.1 |
已知2:几种难溶电解质的溶解度(20℃)
物质 | 溶解度/g |
Fe(OH)2 | 5.2×10-5 |
Fe(OH)3 | 3×10-9 |
MgCO3 | 3.9×10-2 |
Mg(OH)2 | 9×10-4 |
(已知:Fe2+氢氧化物呈絮状,不易从溶液中除去)
请回答:
(1)步骤Ⅱ中加入的试剂X为漂液(含25.2%NaClO)。
①用玻璃棒蘸取漂液滴在pH试纸上,pH试纸先变蓝,后褪色。说明漂液具有的性质是________。
②用化学用语表示NaClO溶液使pH试纸变蓝的原因_________。
③步骤Ⅱ中漂液的主要作用是__________。
④若用H2O2代替漂液,发生反应的离子方程式为_________。
(2)步骤Ⅲ中加入的试剂Y为NaOH,应将溶液的pH调节为______,目的是_______。
(3)步骤Ⅳ中加入的试剂Z为Na2CO3,发生反应的离子方程式为_______。
(4)结合化学用语,应用化学平衡移动原理解释步骤Ⅴ中反应发生的原因_______。


