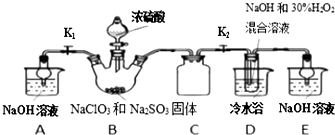
题目内容
6.下列有关NaClO和NaCl混合溶液的叙述正确的是( )| A. | 该溶液中,H+、NH4+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,Ag+、K+、NO${\;}_{3}^{-}$、CH3CHO不能大量共存 | |
| C. | 向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O | |
| D. | 向该溶液中加入浓盐酸,每产生22.4LCl2,转移电子约为6.02×1023个 |
分析 A.氢离子与次氯酸钠反应;
B.银离子与次氯酸钠发生双水解反应,次氯酸钠能够氧化乙醛;
C.NaClO为强碱弱酸盐,水解呈碱性,NaCl为中性,溶液中不存在大量的氢离子;
D.没有告诉在标准状况下,不能使用标准状况下的气体摩尔体积计算.
解答 解:A.H+与NaClO反应生成次氯酸,在溶液中不能大量共存,故A错误;
B.NaClO与Ag+发生双水解反应,NaClO能够氧化CH3CHO,在溶液中不能大量共存,故B正确;
C.NaClO为强碱弱酸盐,水解呈碱性,NaCl为中性,溶液中不存在大量的氢离子,与2Fe2++ClO-+2H+═Cl-+2Fe3++H20反应矛盾,故C错误;
D.由于不是标准状况下,22.4L冷氯气的物质的量不一定为1mol,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,熟练掌握离子反应发生条件,D为易错点,注意明确标准状况下气体摩尔体积的使用条件.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.铁、铜单质及其化合物应用范围很广.现有含氯化亚铁杂质的氯化铜晶体(CuCl2•2H2O),为制取纯净的CuCl2•2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:
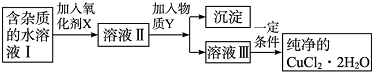
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见表:
(1)最适合作氧化剂X的是C.
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)加入氧化剂的目的是将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离.
(3)加入的物质Y是CuO或Cu(OH)2或CuCO3或Cu2(OH)2CO3(写化学式),目的是调节溶液的pH.根据信息,溶液的pH范围应为调节溶液的pH至4~4.7.
(4)当c(Fe3+)=10-5mol/L时,认为沉淀完全,则Fe(OH)3的Ksp=1×10-35.
(5)结合方程式和必要文字说明解释不能将溶液Ⅲ直接蒸发结晶得到CuCl2•2H2O晶体的原因CuCl2+2H2O?Cu(OH)2+2HCl温度升高,HCl挥发,水解平衡正向移动,得到Cu(OH)2固体,而无法得到晶体.
(6)在饱和氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐溶解,同时还产生的现象有产生气泡和红褐色沉淀.

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 4 | 9.0 | 6.7 |
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)加入氧化剂的目的是将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离.
(3)加入的物质Y是CuO或Cu(OH)2或CuCO3或Cu2(OH)2CO3(写化学式),目的是调节溶液的pH.根据信息,溶液的pH范围应为调节溶液的pH至4~4.7.
(4)当c(Fe3+)=10-5mol/L时,认为沉淀完全,则Fe(OH)3的Ksp=1×10-35.
(5)结合方程式和必要文字说明解释不能将溶液Ⅲ直接蒸发结晶得到CuCl2•2H2O晶体的原因CuCl2+2H2O?Cu(OH)2+2HCl温度升高,HCl挥发,水解平衡正向移动,得到Cu(OH)2固体,而无法得到晶体.
(6)在饱和氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐溶解,同时还产生的现象有产生气泡和红褐色沉淀.
17.下列叙述中,正确的是( )
| A. | 在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 | |
| B. | 得电子越多的氧化剂,其氧化性就越强 | |
| C. | 阳离子只有氧化性,阴离子只有还原性 | |
| D. | 有单质参加的反应不一定属于氧化还原反应 |
11.据悉,奥运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾.撞击时发生反应的化学方程式为:5KClO3+6P═3P2O5+5KCl,则下列有关叙述错误的是( )
| A. | 上述反应是放热反应 | |
| B. | 该反应氧化剂与还原剂物质的量之比为6:5 | |
| C. | 产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾) | |
| D. | 上述反应中消耗3molP时,转移电子的物质的量为15mol |
18.常温下,浓度均为0.1mol•L-1的6种溶液pH如下:
请根据上表数据回答:
(1)常温下,相同物质的量浓度的下列稀溶液,其酸性由强到弱的顺序是B>C>A(用A、B、C表示).
A.H2SiO3 B.H2SO3 C.H2CO3
(2)在上述NaHCO3溶液中加0.1mol•L-1CaCl2,不能产生CaCO3沉淀的原因:HCO3-的电离程度很小,c(CO32-)很小,Qc<Ksp(CaCO3)不能产生沉淀.
(3)6种溶液中,水的电离程度最小的是NaHSO3(填化学式).
(4)若增大氯水中次氯酸的浓度,可向氯水中加入上表中的物质是NaHCO3或NaClO(填化学式).
(5)等浓度的H2SO3和NaHSO3混合液,加入少量的强酸或强碱溶液,pH值都没有明显变化,请解释之.(用离子方程式表示)加碱发生反应:H2SO3+OH-═HSO${\;}_{3}^{-}$+H2O;加酸发生反应:HSO${\;}_{3}^{-}$+H+═H2SO3.
| 溶质 | Na2CO3 | NaHCO3 | Na2SiO3 | Na2SO3 | NaHSO3 | NaClO |
| pH | 11.6 | 9.7 | 12.3 | 10.0 | 4.0 | 10.3 |
(1)常温下,相同物质的量浓度的下列稀溶液,其酸性由强到弱的顺序是B>C>A(用A、B、C表示).
A.H2SiO3 B.H2SO3 C.H2CO3
(2)在上述NaHCO3溶液中加0.1mol•L-1CaCl2,不能产生CaCO3沉淀的原因:HCO3-的电离程度很小,c(CO32-)很小,Qc<Ksp(CaCO3)不能产生沉淀.
(3)6种溶液中,水的电离程度最小的是NaHSO3(填化学式).
(4)若增大氯水中次氯酸的浓度,可向氯水中加入上表中的物质是NaHCO3或NaClO(填化学式).
(5)等浓度的H2SO3和NaHSO3混合液,加入少量的强酸或强碱溶液,pH值都没有明显变化,请解释之.(用离子方程式表示)加碱发生反应:H2SO3+OH-═HSO${\;}_{3}^{-}$+H2O;加酸发生反应:HSO${\;}_{3}^{-}$+H+═H2SO3.