题目内容
一定条件下发生反应N2+ 3H2 2NH3,在5 min内,N2的物质的量浓度由6 mol/ L,变为2 mol / L,则用NH3表示该反应在这段时间的平均速率为
A. 4 mol / (L•min) B. 1.6 mol /(L•min) C. 0.8 mol / (L•min) D. 0.6 mol / (L•min)
B
解析:氮气浓度的变化量是6mol/L-2mol/L=4mol/L,根据变化量之比是相应的化学计量数之比可知氨气浓度的变化量是4mol/L×2=8mol/L。所以其反应速率是
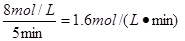 ,答案是B。
,答案是B。

练习册系列答案
相关题目
将2molSO2和2molSO3气体混合于容积一定的密闭容器中,在一定条件下发生反应:2SO2+O2?2SO3,达平衡时SO3为n mol.在相同温度下,按下列配比在该容器中放入起始物质,达平衡时,SO3的物质的量将大于n mol的是( )
| A、2molSO2和1molO2 | B、2molSO2、0.5molO2和molSO3 | C、4molSO2和1molO2 | D、3molSO2、1molO2和1molSO3 |
