题目内容
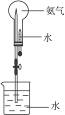
按右图所示的装置和方法进行实验。

(1)实验开始一段时间后,可观察到锥形瓶口上方有白烟生成,请将可能观察到的其他现象补齐:______________________。有关的化学方程式为_________________。
(2)一段时间后,上述实验现象不太明显。为了重新看到明显的现象,需向锥形瓶中加入。( )
(3)经过对比实验证明,在其他条件相同时,用空气代替氧气的实验效果较差,主要原因是_______________________________________________________________________________。

(1)实验开始一段时间后,可观察到锥形瓶口上方有白烟生成,请将可能观察到的其他现象补齐:______________________。有关的化学方程式为_________________。
(2)一段时间后,上述实验现象不太明显。为了重新看到明显的现象,需向锥形瓶中加入。( )
| A.固体NaOH | B.CaO粉末 |
| C.浓H2SO4 | D.H2O |
(1)在锥形瓶中有红棕色气体生成,Pt丝保持红热4NH3+5O2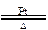 4NO+6H2O 2NO+O2====2NO2 3NO2+H2O====2HNO3+NO HNO3+NH3====NH4NO3 (2)AB (3)空气中含氧气体积分数低,不利于NH3的氧化反应;氮气带走大量热量,不利于NH3的氧化反应
4NO+6H2O 2NO+O2====2NO2 3NO2+H2O====2HNO3+NO HNO3+NH3====NH4NO3 (2)AB (3)空气中含氧气体积分数低,不利于NH3的氧化反应;氮气带走大量热量,不利于NH3的氧化反应
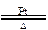 4NO+6H2O 2NO+O2====2NO2 3NO2+H2O====2HNO3+NO HNO3+NH3====NH4NO3 (2)AB (3)空气中含氧气体积分数低,不利于NH3的氧化反应;氮气带走大量热量,不利于NH3的氧化反应
4NO+6H2O 2NO+O2====2NO2 3NO2+H2O====2HNO3+NO HNO3+NH3====NH4NO3 (2)AB (3)空气中含氧气体积分数低,不利于NH3的氧化反应;氮气带走大量热量,不利于NH3的氧化反应(1)浓氨水具有挥发性,挥发出来的NH3与O2以加热的Pt丝为催化剂发生反应:4NH3+5O2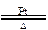 4NO+6H2O(放热反应)。生成的NO继续与O2反应:2NO+O2====2NO2。NO2与挥发出来的H2O反应:3NO2+H2O====2HNO3+NO。HNO3遇到NH3发生反应:HNO3+NH3====NH4NO3。发生的这些反应决定了除能看到瓶口上方有白烟外,还能看到瓶内有红棕色气体生成、Pt丝继续保持红热。(2)一段时间后实验现象不太明显的原因是氨水的浓度降低,挥发出来的NH3减少。要想重新使实验现象明显,必须加入促使NH3挥发的物质。固体NaOH粉末溶于水放出大量热量,且增大溶液中OH-浓度,CaO与H2O反应消耗水,放出大量的热,且增大OH-浓度,能促使NH3挥发,符合要求。浓H2SO4能与氨水反应,不符合要求。加入H2O使氨水浓度降低,不利于NH3的挥发,不符合要求。
4NO+6H2O(放热反应)。生成的NO继续与O2反应:2NO+O2====2NO2。NO2与挥发出来的H2O反应:3NO2+H2O====2HNO3+NO。HNO3遇到NH3发生反应:HNO3+NH3====NH4NO3。发生的这些反应决定了除能看到瓶口上方有白烟外,还能看到瓶内有红棕色气体生成、Pt丝继续保持红热。(2)一段时间后实验现象不太明显的原因是氨水的浓度降低,挥发出来的NH3减少。要想重新使实验现象明显,必须加入促使NH3挥发的物质。固体NaOH粉末溶于水放出大量热量,且增大溶液中OH-浓度,CaO与H2O反应消耗水,放出大量的热,且增大OH-浓度,能促使NH3挥发,符合要求。浓H2SO4能与氨水反应,不符合要求。加入H2O使氨水浓度降低,不利于NH3的挥发,不符合要求。
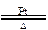 4NO+6H2O(放热反应)。生成的NO继续与O2反应:2NO+O2====2NO2。NO2与挥发出来的H2O反应:3NO2+H2O====2HNO3+NO。HNO3遇到NH3发生反应:HNO3+NH3====NH4NO3。发生的这些反应决定了除能看到瓶口上方有白烟外,还能看到瓶内有红棕色气体生成、Pt丝继续保持红热。(2)一段时间后实验现象不太明显的原因是氨水的浓度降低,挥发出来的NH3减少。要想重新使实验现象明显,必须加入促使NH3挥发的物质。固体NaOH粉末溶于水放出大量热量,且增大溶液中OH-浓度,CaO与H2O反应消耗水,放出大量的热,且增大OH-浓度,能促使NH3挥发,符合要求。浓H2SO4能与氨水反应,不符合要求。加入H2O使氨水浓度降低,不利于NH3的挥发,不符合要求。
4NO+6H2O(放热反应)。生成的NO继续与O2反应:2NO+O2====2NO2。NO2与挥发出来的H2O反应:3NO2+H2O====2HNO3+NO。HNO3遇到NH3发生反应:HNO3+NH3====NH4NO3。发生的这些反应决定了除能看到瓶口上方有白烟外,还能看到瓶内有红棕色气体生成、Pt丝继续保持红热。(2)一段时间后实验现象不太明显的原因是氨水的浓度降低,挥发出来的NH3减少。要想重新使实验现象明显,必须加入促使NH3挥发的物质。固体NaOH粉末溶于水放出大量热量,且增大溶液中OH-浓度,CaO与H2O反应消耗水,放出大量的热,且增大OH-浓度,能促使NH3挥发,符合要求。浓H2SO4能与氨水反应,不符合要求。加入H2O使氨水浓度降低,不利于NH3的挥发,不符合要求。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 CaCO3↓+2HClO?
CaCO3↓+2HClO? +HSO
+HSO ??
??